
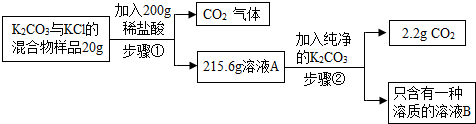
分析 碳酸钾和稀盐酸反应生成氯化钾、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳质量可以计算碳酸钾的质量,同时可以计算稀盐酸的溶质质量分数.
解答 解:(1)步骤①得到的CO2质量是:200g+20g-215.6g=4.4g;
由步骤②产生二氧化碳可知,步骤①中稀盐酸过量,因此溶液A含有的溶质是KCl、HCl.
故填:4.4;KCl、HCl.
(2)设碳酸钾质量为x,
K2CO3+2HCl═2KCl+H2O+CO2↑,
138 44
x 4.4g
$\frac{138}{x}$=$\frac{44}{4.4g}$,
13.8g,
答:K2CO3与KCl混合物样品中K2CO3的质量是13.8g.
(3)设稀盐酸中氯化氢质量为y,
K2CO3+2HCl═2KCl+H2O+CO2↑,
73 44
y 4.4g+2.2g
$\frac{73}{y}$=$\frac{44}{4.4g+2.2g}$,
y=10.95g,
实验中加入的稀盐酸的溶质质量分数是:$\frac{10.95g}{200g}$×100%=5.5%,
故填:5.5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.


科目:初中化学 来源: 题型:选择题
| A. | 液氧(O2)作为助燃剂使用 | |
| B. | 使用硝酸(HNO3),作为农作物生长的氮肥 | |
| C. | 干冰(CO2)用于人工降雨 | |
| D. | 在豆浆中加入石膏(CaSO4),可以制成豆腐 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
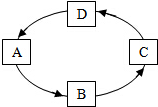 已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.
已知A、B、C、D均为初中化学中最常见的物质,它们之间存在如图所示的转化关系,其中A为最常见的溶剂.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
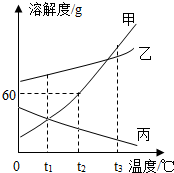 如图为甲、乙、丙三种物质的溶解度曲线,据图回答:
如图为甲、乙、丙三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
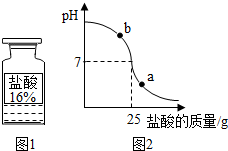
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com