
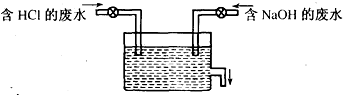
 育才中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含2%HCl,其密度为1.03g/mL,一方排出含4%NaO0H,其密度也为1.03g/mL,然后在池中混合,充分反应后再排放.
育才中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含2%HCl,其密度为1.03g/mL,一方排出含4%NaO0H,其密度也为1.03g/mL,然后在池中混合,充分反应后再排放.  =
=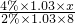 ,解得x=4.4L/s
,解得x=4.4L/s

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 育才中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含2%HCl,其密度为1.03g/mL,一方排出含4%NaO0H,其密度也为1.03g/mL,然后在池中混合,充分反应后再排放.
育才中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含2%HCl,其密度为1.03g/mL,一方排出含4%NaO0H,其密度也为1.03g/mL,然后在池中混合,充分反应后再排放. 查看答案和解析>>
科目:初中化学 来源:化学教研室 题型:058
某中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含
2%的HCl,其密度为1.03g/mL的废水,另一方排出含4%的NaOH,其密度也为1.03g/mL的废水,然后在池中混合,充分反应后再排放.请你回答下列问题: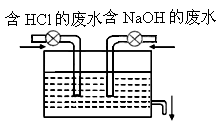
(1)
当处理后废水pH为8时,此时控制含NaOH的废水的阀门应调__________(填“大”或“小”).(2)
当处理后的废水pH约为7时,如果把含HCl的废水流量为8L/s,则含NaOH废水的流量约为__________L/s(精确到小数点后一位).
查看答案和解析>>
科目:初中化学 来源: 题型:038
某中学实验室模拟工厂治污原理,设计了如下图的装置,一方排出含
2%的HCl,其密度为1.03g/mL的废水,另一方排出含4%的NaOH,其密度也为1.03g/mL的废水,然后在池中混合,充分反应后再排放.请你回答下列问题: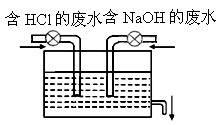
(1)
当处理后废水pH为8时,此时控制含NaOH的废水的阀门应调__________(填“大”或“小”).(2)
当处理后的废水pH约为7时,如果把含HCl的废水流量为8L/s,则含NaOH废水的流量约为__________L/s(精确到小数点后一位).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com