
 某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究.
某学习小组对课本中“食盐常用于制氯气、烧碱”的内容产生兴趣.在老师的指导下,用自制的实验装置(主体部分如图所示)进行电解饱和食盐水制取氢氧化钠的实验.一段时间后,关闭电源,从K处导出部分的溶液作为待测液进行如下探究.| 实验步骤 | 实验现象 | 实验结论 |
| 取样,滴加几滴无色酚酞试液 | 溶液变红色 | 待测液中含有氢氧化钠. |
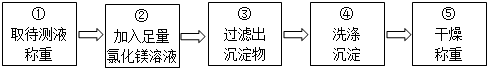
分析 (1)氢氧化钠溶液显碱性,能使酚酞试液变红色;
(2)为了使氢氧化钠溶液中的氢氧化钠和氯化镁完全反应,氯化镁溶液应该是足量的;
(3)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,因此步骤③过滤出的沉淀物是氢氧化镁;
(4)利用沉淀物的质量计算氢氧化钠的质量分数时,若不洗涤沉淀,那么沉淀上会附着一些杂质,从而使沉淀的质量增大,会导致计算出的氢氧化钠质量偏大,使所测定氢氧化钠的质量分数偏大.
解答 解:(1)
实验步骤:向待测液中滴加几滴酚酞试液;
实验现象:酚酞试液变红色;
实验结论:待测液中含有氢氧化钠;
(2)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应;
步骤④中判断沉淀物是否洗净的具体操作:取最后一次洗涤液少许于试管中,滴加硝酸银溶液,若无白色沉淀生成,说明沉淀物已洗净,反之则没有洗;
(3)氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,步骤②中发生反应的化学方程式是2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(4)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,沉淀中因含有其他杂质而质量偏大,所测定氢氧化钠的质量分数将偏大.
故答案为:
答案:
探究活动一
(1)取样,滴加几滴无色酚酞试液;溶液变红色(此题其他合理答案也可);
探究活动二
(2)使NaOH完全反应;滴加硝酸银溶液,若无白色沉淀生成,说明沉淀物已洗净,反之则没有洗净.(或其他合理答案)
(3)2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(4)偏大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:推断题
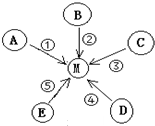 如图所示,A、B均为纯净物,C、D、E均为混合物;①--⑤五条途径(如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,工业上可通过途径④来生产M,自然界可通过途径⑤来提供M;途径①、②、③反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.
如图所示,A、B均为纯净物,C、D、E均为混合物;①--⑤五条途径(如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,工业上可通过途径④来生产M,自然界可通过途径⑤来提供M;途径①、②、③反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管,滴加滴加氯化钙溶液. | 产生白色沉淀 | 该溶液是碳酸钠溶液.有关反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①③⑤ | C. | ①③④⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用食醋可除去热水瓶胆的水垢,是由于食醋具有酸性 | |
| B. | 炭黑常用来作炭素墨水,是由于炭黑为黑色且常温下化学性质稳定 | |
| C. | 浓硫酸可用作干燥剂,是由于浓硫酸具有脱水性 | |
| D. | 稀有气体中的氦气可用于填充气球,是由于氦气密度小且化学性质稳定. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com