
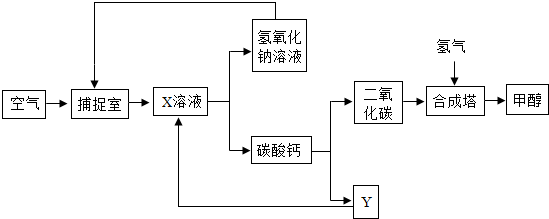
分析 (1)根据二氧化碳与氢氧化钠反应的反应物、生成物写出化学方程式;
(2)将Y加入X溶液后发生的化学方程式有:氧化钙溶于水生成氢氧化钙,然后氢氧化钙与碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠,所以通过过滤可以将其分离开来;
(3)可循环使用的物质是在前面的反应物中出现过,到了后面的生成物中又出现该物质;
(4)根据合成塔内的反应条件为300℃,200kPa和催化剂,写出合成塔内反应的化学方程式.
解答 解:(1)捕捉室中发生反应的化学反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,其化学方程式为CO2+2NaOH=Na2CO3+H2O.
故答案是:CO2+2NaOH=Na2CO3+H2O;
(2)CaO和水反应生成氢氧化钙,其反应方程式为:CaO+H2O=Ca(OH)2;然后氢氧化钙与碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠,其反应方程式为:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;固体与液体分开用过滤,过滤需要用到的玻璃仪器有:烧杯、量筒、玻璃棒等,故答案是:CaO+H2O=Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;烧杯;
(3)碳酸钠和氢氧化钙反应生成了碳酸钙和氢氧化钠,而在前面空气和氢氧化钠反应生成碳酸钠,所以氢氧化钠可以循环使用;碳酸钙高温生成了氧化钙和二氧化碳,在前面氧化钙与碳酸钠溶液反应,所以氧化钙也可以循环使用,故填:NaOH;CaO;
(4)合成塔内的反应条件为300℃,200kPa和催化剂,合成塔内反应的化学方程式为:3H2+CO2$\frac{\underline{\;300℃、200KPa\;}}{催化剂}$CH3OH+H2O;
故答案为:
(1)2NaOH+CO2=Na2CO3+H2O
(2)CaO+H2O=Ca(OH)2; Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;烧杯;
(3)NaOH;CaO;
(4)3H2+CO2$\frac{\underline{\;300℃、200KPa\;}}{催化剂}$CH3OH+H2O.
点评 解答本题关键是会书写化学方程式,要知道可循环使用物质的找法,前面反应物中出现,后面的生成物中出现.


 特高级教师点拨系列答案
特高级教师点拨系列答案科目:初中化学 来源: 题型:选择题
| 温度/℃ | 0 | 10 | 20 | 30 |
| 物质a溶解度/g | 2 | 5 | 10 | 20 |
| 物质b溶解度/g | 7 | 8 | 10 | 14 |
| A. | 30℃时物质a的饱和溶液,降温到10℃时变成不饱和溶液 | |
| B. | 30℃时物质b的饱和溶液,降温到20℃时溶质质量分数减小 | |
| C. | 30℃时,向100g水中加入25g物质a,充分溶解后所得溶液是饱和溶液 | |
| D. | 30℃时,要将物质b的不饱和溶液转变为饱和溶液,可以采取恒温蒸发水的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 物质(纯净物) | 乙醇 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 2.3 | 4 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 2.2 | 2.7 | 待测 |
| A. | 反应后X的质量为1.4g | B. | X中一定含有碳元素和氢元素 | ||
| C. | X中一定含有碳元素和氧元素 | D. | X中两种元素的质量比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 从微观上看,物质是由分子、原子或离子构成 | |
| B. | 化学变化的微观实质是分子的破裂和原子的重组 | |
| C. | 金刚石和石墨物理性质不同的原因是碳原子的排列方式不同 | |
| D. | 酸有一些相似的化学性质,是因为在不同的酸溶液都具有酸根离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KH2PO4属于氧化物 | B. | KH2PO4中磷元素的化合价为+4 | ||
| C. | KH2PO4的相对分子质量为136 | D. | KH2PO4中氢、氧元素的质量比为1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 制取气体时,先装药品,后检查装置的气密性 | |
| B. | 加热高锰酸钾并用排水法收集氧气实验结束时,先熄灭酒精灯,后移出导管 | |
| C. | 加热试管时,先使试管底部均匀受热,后用酒精灯的外焰固定加热 | |
| D. | 一氧化碳还原氧化铁实验结束时,先停止通一氧化碳,过段时间后停止加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com