
| A. | 纯碱 火碱 Na2CO3 | B. | 熟石灰 氧化钙 CaO | ||
| C. | 生石灰 碳酸钙 CaCO3 | D. | 火碱 氢氧化钠 NaOH |
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:初中化学 来源: 题型:填空题
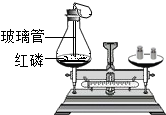 质量守恒定律的探究实验(一)--红磷燃烧实验.实验装置如图.
质量守恒定律的探究实验(一)--红磷燃烧实验.实验装置如图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作步骤 | 实验现象 | 结论 |
| 步骤一:另取少量滤液于另一支试管中,滴加碳酸钠溶液. | 实验过程中产生白色沉淀. | 猜想2正确 |
| 步骤二:取少量滤液于试管中,滴加稀盐酸,振荡. | 无明显现象 | 猜想3不正确. |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2.8g | B. | 5.6g | C. | 11.2g | D. | 1.4g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事 实 | 解 释 |
| A | 水汽化所占体积变大 | 水分子由液态变成气态 |
| B | 碳酸钠溶液和碳酸钾溶液都能和盐酸反应 | 它们都含有碳酸根离子 |
| C | 6000L的氧气可以压缩到40L的钢瓶中 | 氧气分子间的间隔比较大 |
| D | 一氧化碳和二氧化碳的化学性质不同 | 它们的分子结构不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
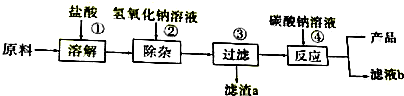
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 绿色植物光合作用 | |
| B. | 铜丝导电 | |
| C. | 装有澄清石灰水的试剂瓶内壁有白膜 | |
| D. | 着火点40摄氏度左右的白磷保存在水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com