
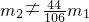 ,则原样品一定含有杂质
,则原样品一定含有杂质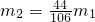 ,则原样品一定不含有杂质
,则原样品一定不含有杂质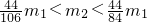 ,则原样品一定含有NaHCO3,可能含有K2CO3
,则原样品一定含有NaHCO3,可能含有K2CO3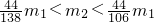 ,则原样品一定含有K2CO3,不可能含有NaHCO3
,则原样品一定含有K2CO3,不可能含有NaHCO3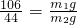

 =
=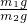
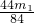
 =
=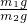

 ,若m2≠
,若m2≠ ,则说明样品中含有杂质,故A正确;
,则说明样品中含有杂质,故A正确; 也可能成立,故B不正确;
也可能成立,故B不正确;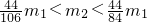 ,则此时混有的杂质一定含有碳酸氢钠,否则产生二氧化碳气体的质量不可能大于
,则此时混有的杂质一定含有碳酸氢钠,否则产生二氧化碳气体的质量不可能大于 ,混有极少量的碳酸钾也不会影响产生二氧化碳气体的质量,所以混合物可能含有碳酸钾,故C正确;
,混有极少量的碳酸钾也不会影响产生二氧化碳气体的质量,所以混合物可能含有碳酸钾,故C正确;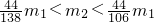 ,则原样品一定含有K2CO3,当然也可能含有碳酸氢钠,故D不正确.
,则原样品一定含有K2CO3,当然也可能含有碳酸氢钠,故D不正确.

科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:云南省中考真题 题型:实验题
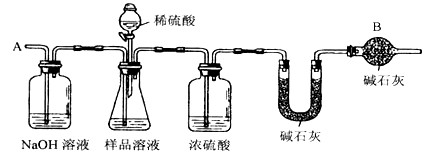
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com