
分析 (1)含碳物质不充分燃烧会产生黑烟;
(2)根据物质的变化形式来分析;
(3)煤的直接液化是煤在高温和催化剂存在下与H2O作用生成液体燃料的过程;
(4)据质量守恒判断x的化学式;
(5)根据化合价升降总数相等以及原子守恒来写离子方程式;
(6)根据氨氧化的化学方程式来分析;根据题干信息分析O2浓度对平衡的影响.
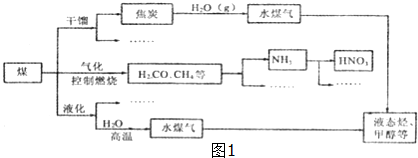
解答 解:(1)如果燃烧时氧气不充足,会不完全燃烧,有碳颗粒生成,会有黑烟产生,故答案为:燃烧时氧气不充足;
(2)煤经过干馏得到新物质--焦炉气、煤焦油和焦炭等,所以发生的属于化学变化,故填:化学;
(3)煤的直接液化是煤与适当溶剂混合后在高温和催化剂存在下与H2O作用生成液体燃料的过程,故答案为:催化剂;水;
(4)根据化学方程式和质量守恒定律分析,反应前K:1个,反应后:1个,则x中不含K;反应前Al:1个,反应后应:1个,则x中含有一个Al,依此类推,x中还含有3个O,3个H,则X的化学式为 Al(OH)3,故答案为:Al(OH)3;
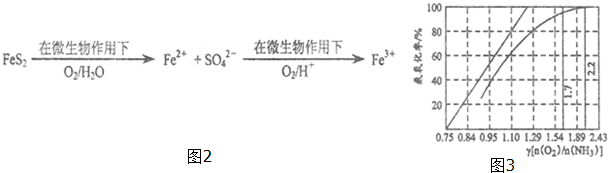
(5)第一步反应中反应物有FeS2、O2和H2O,生成物有Fe2+和${SO}_{4}^{2-}$,反应的方程式为:2FeS2+7O2+2H2O$\frac{\underline{\;微生物\;}}{\;}$2H2SO4+2FeSO4;Fe2+具有还原性,可被氧气氧化为Fe3+,方程式为:2H2SO4+O2+4FeSO4$\frac{\underline{\;微生物\;}}{\;}$2Fe2(SO4)3+2H2O;故填:2FeS2+7O2+2H2O$\frac{\underline{\;微生物\;}}{\;}$2H2SO4+2FeSO4;2H2SO4+O2+4FeSO4$\frac{\underline{\;微生物\;}}{\;}$2Fe2(SO4)3+2H2O;
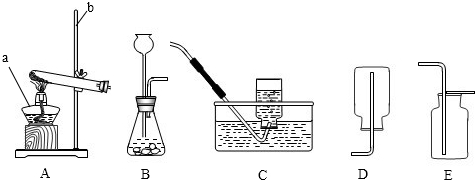
(6)结合题干信息:由氨氧化的化学方程式:4NH3+5O2$\frac{\underline{\;高温高压\;}}{催化剂}$4NO+6H2O,可知氨氧化率达到100%,实际生产要将γ值维护在1.7-2.2之间,原因是浓度太少不利于NH3的转化,γ值为2.2时NH3氧化率已近100%,故答案为:O2浓度太少不利于NH3的转化,γ值为2.2时NH3氧化率已近100%.
点评 本题考查煤的综合利用,涉及到氧化还原方程式的书写,题目难度中等,本题注意从题目中获取信息,结合物质的性质解答.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案科目:初中化学 来源: 题型:选择题
| A. | 不能产生氧气 | B. | 产生氧气的速率慢 | ||
| C. | 产生氧气的总量减少 | D. | 没有氯化钾生成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
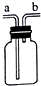 如图装置既可以用于排空气法又可以用于排水法收集气体.无论瓶内装满空气还是装满水,收集气体时,制的气体都从b端进入,该气体是( )
如图装置既可以用于排空气法又可以用于排水法收集气体.无论瓶内装满空气还是装满水,收集气体时,制的气体都从b端进入,该气体是( )| A. | O2 | B. | CO2 | C. | H2 | D. | CO |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 请根据物质与其构成粒子之间的关系回答下列问题:
请根据物质与其构成粒子之间的关系回答下列问题: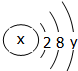
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com