
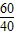 =
=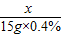
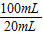 =0.45g
=0.45g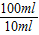 =4.5g
=4.5g

科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:连云港 题型:问答题
查看答案和解析>>
科目:初中化学 来源: 题型:
国家规定,酿造食醋总酸含量不得低于3.5g/100 mL(总酸含量即100 mL食醋中含醋酸的质量)。某兴趣小组为测定一市售食用白醋的总酸含量,进行了如下实验:
首先取10 mL该白醋样品,稀释至 100 mL;然后,取稀释后的溶液20 mL用溶质质量分数为0.4%的NaOH溶液中和,当消耗NaOH溶液15g时,恰好完全反应(醋酸与氢氧化钠反应的化学方程式为:CH3COOH+NaOH=CH3COONa+H2O,假设其他物质不与氢氧化钠反
应)。
计算:(1)20mL稀释后的溶液中醋酸的质量;
(2)该市售白醋样品中的总酸含量,并说明是否符合国家标准。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com