
分析 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比;根据葡萄糖的化学式为C6H12O6,水是H2O,从化学式可以看出不管葡萄糖与水如何混合,在溶液中氢元素和氧元素的质量比总是H:O等于1:8.据此分析解答.
解答 解:葡萄糖是由碳、氢、氧三种元素的质量比为(12×6):(1×12):(16×6)=6:1:8.
根据葡萄糖的化学式为C6H12O6,水是H2O,从两者的化学式可以看出不管葡萄糖与水如何混合,在溶液中,氢元素和氧元素的质量比总是H:O等于1:8,葡萄糖溶液中C元素的质量分数是1%,设溶液中H元素的质量分数是x,氧元素的质量分数为8x,则葡萄糖溶液中1%+x+8x=100%,所以x=11%;
故答案为:6:1:8;11%.
点评 主要考查了相对分子质量的计算方法,元素质量分数的求法以及利用相对质量求物质中所含元素的比值的方法,掌握化学式的基本计算是解题的关键.


科目:初中化学 来源: 题型:计算题
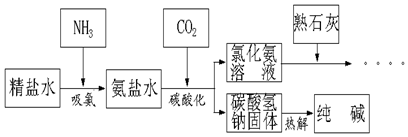
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
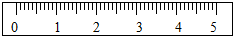
| 砝码/g | 50 | 20 | 20 | 10 | 5 |
| 取用情况 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 向某无色溶液中滴入硫酸试液,产生白色沉淀,证明该溶液是氯化钡溶液 | |
| B. | 向某无色溶液中滴入硫酸铜溶液,产生蓝色沉淀,证明该溶液是氢氧化钠 | |
| C. | 某白色固体与熟石灰混合后加热,产生可使湿润红色石蕊试纸变蓝色的气体,证明该白色固体是铵盐 | |
| D. | 把燃着的木条伸入某无色气体的集气瓶中,火焰熄灭,证明该气体是二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③ | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4、NaCl、HCl | B. | H2SO4、HCl、NaOH | ||
| C. | CaCl2、Na2CO3、K2CO3 | D. | FeCl3、NaOH、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
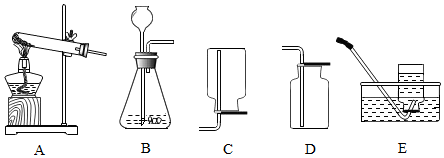
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| Na2CO3 | 7 | 21.8 | 48.8 | 46.4 | 45.1 | 44.7 |
| NaCI | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com