
| A. | 铁、锌各4g | B. | 铁、锌各5g | C. | 铁、锌各6g | D. | 铁、锌各7g |
分析 如果酸过量金属完全反应,则相同质量的不同金属与同质量的酸反应后生成气体的质量肯定不同,天平不能保持平衡;如果金属过量酸完全反应,产生H2的质量必相同,此时天平必保持平衡.
解答 解:设向两个烧杯中同时分别加入铁的质量为x、锌的质量为y,
Fe~H2SO4
56 98
x 100g×9.8%
$\frac{56}{x}$=$\frac{98}{100g×9.8%}$
x=5.6g
Zn~H2SO4
65 98
y 100g×9.8%
$\frac{65}{y}$=$\frac{98}{100g×9.8%}$
x=6.5g
因为要想反应完全后,天平仍保持平衡,需要铁、锌与100g9.8%的硫酸溶液发生化学反应后生成的氢气同样多,即需要的硫酸溶液同样多,所以加入的铁≥5.6g、锌≥6.5g;
故选:D.
点评 本题考查了质量守恒定律及其应用、根据化学反应方程式的计算,注意解题的规范性和准确性.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
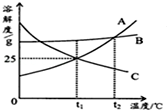
| A. | t1℃时,A的饱和溶液中溶质质量分数为20% | |
| B. | t2℃时A、B、C的溶解度大小为A=B>C | |
| C. | t2℃时等质量的饱和溶液中溶剂质量:C>A=B | |
| D. | t2℃A、B、C的饱和溶液降温到t1℃时,A、C两溶液中溶质的质量分数相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
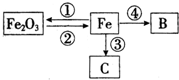 构建知识网络是一种重要的学习方法.图是关于铁化学性质的知识网络,其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
构建知识网络是一种重要的学习方法.图是关于铁化学性质的知识网络,其中B是密度最小的气体,C为红色固体单质.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg和NaOH | B. | Na2SO4和MgCl2 | C. | CaO和Fe粉 | D. | 石灰石和Ag |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
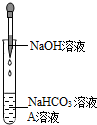 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com