
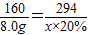
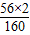 ×100%=5.6g,所以硫元素的质量=12g-5.6g=6.4g
×100%=5.6g,所以硫元素的质量=12g-5.6g=6.4g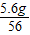 :
: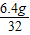 =1:2,则硫铁矿主要成分的化学式可表示为FeS2;
=1:2,则硫铁矿主要成分的化学式可表示为FeS2;

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:初中化学 来源: 题型:
 (2011?呼和浩特)将相同体积,相同溶质质量分教的稀盐酸,分别加入到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中(金属完全反应〕,生成H2的质量与反应时间的关系如下图所示.下列说法中正确的是( )
(2011?呼和浩特)将相同体积,相同溶质质量分教的稀盐酸,分别加入到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中(金属完全反应〕,生成H2的质量与反应时间的关系如下图所示.下列说法中正确的是( )查看答案和解析>>
科目:初中化学 来源: 题型:
 (2011?呼和浩特)人类生活和工农业生产都离不开水,右图是自来水厂净化水的过程示意图:
(2011?呼和浩特)人类生活和工农业生产都离不开水,右图是自来水厂净化水的过程示意图:查看答案和解析>>
科目:初中化学 来源: 题型:
 (2011?呼和浩特)有一混合溶液是由稀硝酸、碳酸钾溶液、稀硫酸、氯化铜中的两种简单混合而成(两种溶液不反应),向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图:
(2011?呼和浩特)有一混合溶液是由稀硝酸、碳酸钾溶液、稀硫酸、氯化铜中的两种简单混合而成(两种溶液不反应),向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com