
| A. | 一个丙氨酸分子中共含有13个原子 | |
| B. | 丙氨酸中氢元素的质量分数最大 | |
| C. | 一个丙氨酸分子中含有一个氧分子 | |
| D. | 丙氨酸中C、H、O、N三种原子的质量比为3:7:2:1 |
分析 A.根据分子结构来分析;
B.根据化合物中元素的质量比来分析;
C.根据分子的构成来分析;
D.根据化合物中元素质量比的计算方法来分析.
解答 解:A.由丙氨酸的化学式可知,每个丙氨酸分子中含有3个碳原子、7个氢原子、2个氧原子和1个氮原子,共13个原子,故正确;
B.丙氨酸中碳、氢、氧、氮元素的质量比=(12×3):(1×7):(16×2):14=36:7:32:14,可见其中,碳元素的质量分数最大,故错误;
C.1个丙氨酸分子中含有2个氧原子,不含有氧分子,故错误;
D.丙氨酸中碳、氢、氧、氮元素的质量比=(12×3):(1×7):(16×2):14=36:7:32:14,故错误.
故选A.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:初中化学 来源: 题型:实验探究题
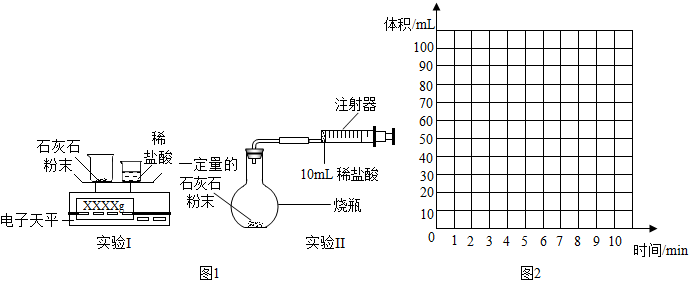
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
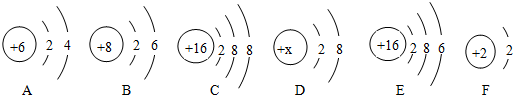
| A. | 都是带电荷的粒子 | B. | 都是保持物质化学性质的最小粒子 | ||
| C. | 都是化学变化中的最小粒子 | D. | 都是构成物质的基本粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
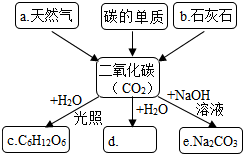 如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略).请按下列要求填空:
如图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略).请按下列要求填空:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水倒流 | B. | 温度过高 | C. | 仪器损坏 | D. | 反应过慢 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com