
【题目】物质之间转化(元素化合物),A~M均为初中化学常见物质,其中A是大理石主要成分;B是人体胃酸的一种主要成分;F是澄清石灰水主要成分;E是钠盐,其水溶液呈碱性;它们之间有如图所示的相互转换关系(图中部分生成物已略去).
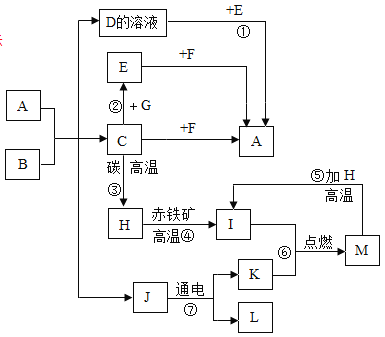
请回答下列问题:
(1)E的俗称为_____(填其中一个)。
(2)写出通电电解J时化学方程式_____,在电解的过程中通常加入少量烧碱或硫酸的目的是增强J物质的_____(填一物理性质)。
(3)实验室进行有关反应④的实验,当固体全部转化为生成物时,固体颜色由_____色变为_____色。
(4)反应①-⑦中不涉及的基本反应类型是_____反应(填“化合”“分解”“置换”或“复分解”)。
(5)请写出⑤的化学方程式_____。
(6)为了除去D溶液中少量的B物质,可向溶液中加入过量的_____(从A或F中选择填入所加物质对应的英文序号),然后过滤,所得滤液即为纯净的D溶液。
【答案】纯碱或苏打 ![]() 导电性 红 黑 置换
导电性 红 黑 置换 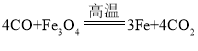 A
A
【解析】
由题干条件可知A为CaCO3,B为HCl,F是Ca(OH)2,A和B反应生成J能通电分解,则J为水,D为CaCl2,C为CO2,CO2与Ca(OH)2生成沉淀A CaCO3,CaCl2能与E反应生成CaCO3,E是钠盐,其水溶液呈碱性,故E为Na2CO3,CO2能与氢氧化钠溶液反应生成碳酸钠,则G为氢氧化钠,CO2能与碳在高温条件下生成CO,则H为CO,CO可以与氧化铁高温条件下反应生成Fe和二氧化碳,则I为Fe,Fe能与氧气反应生成Fe3O4,M是Fe3O4,电解水生成氢气和氧气,则K是O2,L是H2。
(1)E是碳酸钠,俗称是纯碱或苏打。
(2)电解水生成氢气和氧气,化学方程式为![]() ;在电解的过程中通常加入少量烧碱或硫酸的目的是增强水的导电性。
;在电解的过程中通常加入少量烧碱或硫酸的目的是增强水的导电性。
(3)实验室进行一氧化碳高温下还原氧化铁实验时,生成铁和二氧化碳,固体粉末由红色变为黑色。
(4)由题中转化关系可知:①为复分解反应;②不属于四大基本反应;③为化合反应;④为还原反应,不属于四大基本反应;⑤为还原反应,不属于四大基本反应;⑥为化合反应;⑦为分解反应,故①~⑦中不涉及四大基本反应中的置换反应;
(5)反应⑤为一氧化碳和四氧化三铁高温条件下生成铁和二氧化碳,反应的化学方程式为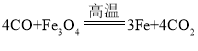 ;
;
(6)除去CaCl2溶液中含少量HCl,可加入过量的A(CaCO3),碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,过量的CaCO3过滤即可除去。


科目:初中化学 来源: 题型:
【题目】以甲为原料合成化工产品丁的微观过程如下图,下列说法正确的是
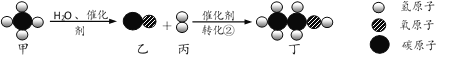
A. 转化①属于置换反应B. 转化②中乙和丙的分子个数之比为1∶3
C. 一定浓度的丁溶液可作消毒剂D. 转化过程中元素化合价无变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请回答下列有关燃烧的问题:
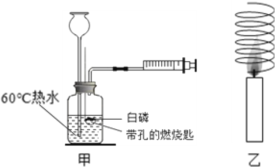
(1)用如图甲所示装置,热水中的白磷不燃烧,但当用注射器向瓶内推入空气,瓶内水面下降,当白磷露出水面时立即燃烧,说明可燃物燃烧的条件是_______,白磷燃烧的化学方程式为________________。
(2)如图乙将一根铜丝烧成螺旋状网罩罩在一支燃着蜡烛的火焰处,不多久蜡烛火焰熄灭,其熄灭的原因是___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类宝贵的自然资源,我们应该了解有关水的知识。
(1)有一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式为_____。
(2)溶液在生产和生活中有着广泛的应用。某同学配制溶液时,在用量筒量取水的过程中俯视读数,这样配制得到的溶液的溶质质量分数会_____(填“偏大”“偏小”或“无影响”)。
(3)A1与NaOH溶液反应会生成NaA1O2和H2,该反应的化学方程式为_____;已知化学反应前后元素化合价发生改变的属于氧化还原反应,反应物中,元素化合价升高被氧化是还原剂,化合价降低被还原是氧化剂,则该反应中H2O是_____(填氧化剂,还原剂)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙烯(C2H4)是一种催熟水果的激素。一定质量的乙烯在不充足的氧气中燃烧,生成物只有CO、CO2和H2O,且总质量为120g,其中H2O 36g,则CO的质量为_____;该反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )
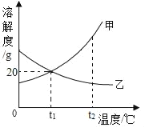
A. t1℃时,甲乙的溶解度相等,它们饱和溶液的溶质质量分数也相等,都为20%
B. t1℃时,30g甲加入到50g水中最多可得80g溶液
C. t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲>乙
D. t2℃,等质量的甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液质量的大小关系为:甲>乙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硒元素在有机体的生命活动过程中具有重要的生物学作用,是人体必需的15种每日膳食营养元素之一,硒缺乏与人类许多疾病的发生有密切关系。同时硒元素过多也可以引起毒性作用。如图为硒在元素周期中的信息,下列所获取的信息中错误的是( )
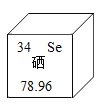
A.硒的核电荷数为34B.硒的元素符号为Se
C.硒是一种金属元素D.硒的相对原子质量为78.96
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人体胃液中含有的酸是_______________。右图是沾有污渍的某抗酸的部分说明,同学们对此展开了系列研究。

Ⅰ.服用方法探究:为什么嚼碎后服用?你认为需后服用的自的是____________。
Ⅱ.抗酸原理探究:
(1)含有NaHCO3相Al(OH)3的药片都能用于治疗胃酸过多,反应原理用方程式可表示为(任写一个)_______________。
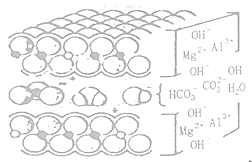
(2)查阅资料可知铝碳酸镁是层状结构(如图),则铝碳酸镁中起到抗酸作用的微粒的符号有____。
Ⅲ.主成分探究:
(查阅资料)铝碳酸镁片加感分解的产物为Al2O3、MgO、CO2和H2O,药品中的其它成分受不分解。
(实验过程)学习小设计了如下图的实验探究铝碳酸镁片的组成。

(1)检查装置气密性,取8.6g该药片,研成粉末放入硬质玻璃管中;
(2)实验开始前先通入一定量空气,然后称量装置D的质量;
(3)点燃消精灯加热。充分反应后,停让加热;
(4)通入空气至玻璃管冷却,目的是防止液体倒吸和___________,然后测得装置D增重0.44g。
(实验结论)铝碳酸镁的化学式为____________。药片中铝碳酸镁的质量分数是________。
(拓展延伸)有医生生建议患有严重胃胀、胃溃疡的患者最好慎用该药而改服氢氧化铝片,试用你学的知识解释这样建议的理由是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请按照要求完成下列金属性质的探究:
探究一:铝片与盐酸反应过程中的能量及反应速率的变化。
(1)实验时需将铝片进行打磨,其目的是_____。
(2)反应中试管外壁发烫,说明铝与盐酸反应是_____(填“吸热”或“放热”)反应,化学方程式为_____。
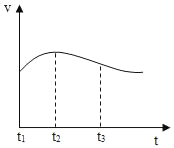
(3)实验测得铝片产生气体的速率(v)与时间(t)的关系如图所示,t1~t2时间内反应逐渐加快的主要原因是_____。
(查阅资料)铁、铜均能与氯化铁溶液反应,化学方程式分别为:2FeC13+Fe═3FeCl2、2FeCl3+Cu=2FeCl2+CuCl2
(4)向氯化铁和氯化铜的混合溶液中,加入一定量的铁粉,充分反应后过滤。取少量滤渣加入稀盐酸,有气泡产生。则滤液中的溶质是_____,滤渣中一定含有_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com