
 实验与探究是化学学习的重要方法和内容.
实验与探究是化学学习的重要方法和内容.| 操作步骤 | 现象记录 | 反应的化学方程式 |
| 取两支试管,分别往试管中加入2mL样品1、2,再往其中滴入盐酸 | 样品1:无明显现象 | NaOH+HCl=NaCl+H2O |
| 样品2:溶液中出现气泡 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
分析 (1)①根据氢氧化钠+稀盐酸→氯化钠+水,碳酸钠+稀盐酸→氯化钠+水+二氧化碳↑书写反应方程式;
②根据用pH试纸测定所配制溶液的pH值的方法进行分析;
(2)根据酚酞试液遇酸不变色,与碱变红色.稀盐酸与氢氧化钠反应生成氯化钠和水,与碳酸钠反应生成氯化钠、水和二氧化碳气体进行分析.
解答 解:(1)①稀盐酸与氢氧化钠反应生成氯化钠和水,与碳酸钠反应生成氯化钠、水和二氧化碳气体,其反应方程式为:
样品1:NaOH+HCl=NaCl+H2O;
样品2:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
②用pH试纸测定所配制溶液的pH值的方法是:在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,即可得出该溶液的pH值;
(2)碳酸钠溶液、氢氧化钠溶液都显碱性,所以它们都能使无色酚酞试液变红;稀盐酸显酸性,不能使无色酚酞试液变色.
所以,步骤一中,C无明显现象,说明C是稀盐酸;A、B溶液的颜色变成红色,说明A、B溶液是碳酸钠溶液、氢氧化钠溶液;
步骤二中,“A、B溶液的颜色由红色变成无色”说明这两种溶液均与稀盐酸反应,“B溶液中有气泡冒出”说明B溶液中含有碳酸根.故B是碳酸钠.
经过推断可知A是氢氧化钠,根据②中的“氢氧化钠溶液浓度过大”造成的异常现象和稀盐酸与氢氧化钠反应生成氯化钠和水可以推断,此时溶液中含有的溶质主要是氯化钠、氢氧化钠.
故答案为:(1)①NaOH+HCl=NaCl+H2O,Na2CO3+2HCl=2NaCl+H2O+CO2↑;
②用玻璃棒蘸取碳酸钠溶液滴在pH试纸上,把试纸呈现的颜色与标准比色卡对照;
(2)①、碳酸钠溶液、稀盐酸;
②氯化钠、氢氧化钠.
点评 掌握中和反应的概念及其应用;掌握pH试纸测定溶液的pH时的操作方法.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
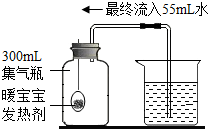 暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).以下对此改进实验的叙述,错误的是( )
暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).以下对此改进实验的叙述,错误的是( )| A. | 发热剂属于混合物 | |
| B. | 此实验的原理是利用铁生锈消耗氧气 | |
| C. | 此实验所取发热剂过多 | |
| D. | 发热剂中的食盐可以缩短实验时间 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 根据如图所示装置(夹持装置已略去)分别进行实验
根据如图所示装置(夹持装置已略去)分别进行实验查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com