
 硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:
硫酸是常见的酸,也是常用的化工原料.由于浓度不同,浓硫酸与稀硫酸在性质上存在较大差异,如浓硫酸具有脱水性、吸水性和强腐蚀性等.某课外兴趣小组为了探究浓硫酸的某些特性做了如下一些实验.请结合有关实验,按要求回答下列问题:分析 (1)依据浓硫酸具有的脱水性与吸水性进行分析判断;
(2)①根据浓硫酸的稀释过程的操作要领分析解答;
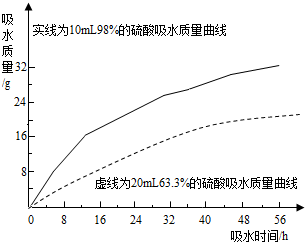
②从曲线观察两种不同的酸的吸水情况的变化趋势分析解答
解答 解:(1)浓硫酸具有的脱水性与吸水性,除去氢气或氧气中的水分,是利用其吸水性,起到干燥剂的作用;
(2)①浓硫酸的稀释时应酸入水并不断搅拌使溶解时产生的热量尽快散失;
②从曲线观察两种不同的酸的吸水情况的变化可知:浓硫酸和一定浓度以上的稀硫酸都具有吸水性,故A错误;
浓硫酸吸水能力比稀硫酸强(吸水速度快、吸水量大),故B正确;
开始两者吸水速度差异比较大,随着时间的推移吸水速度越来越接近,吸水能力越来越弱,故C错误;
硫酸浓度越稀吸水性越弱,到一定浓度后就失去吸水性,故D正确.
故答案为:(1)吸水;
(2)①浓硫酸,水; ②B、D.
点评 该题属于实验方案的探究题,主要是采用对比实验的方法对实验中的问题进行探讨,掌握设计实验的目的及方法是解题的关键所在.


科目:初中化学 来源: 题型:选择题
| A. | NaOH、HCl、CuSO4、MgSO4 | B. | KNO3、HCl、NaCl、NaOH | ||
| C. | Na2CO3、K2SO4、BaCl2、HCl | D. | 酚酞、H2SO4、NaOH、MgCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜片插入稀硫酸:Cu+H2SO4═CuSO4+H2↑ | |
| B. | 工业炼铁:FexOy+yCO$\frac{\underline{\;高温\;}}{\;}$xFe+yCO2 | |
| C. | 氢氧化钠溶液吸收二氧化硫:2NaOH+SO2═Na2SO4+H2O | |
| D. | 二氧化碳通入氯化钙溶液:CO2+CaCl2+H2O═CaCO3↓+2HCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在实验学习过程时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.
在实验学习过程时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的研究.| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加少量硫酸铜(氯化铜)溶液; | 溶液中出现蓝色沉淀 | 猜想①正确. 反应方程式为: |
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,而后先滴加少量无色酚酞试液,再加入过量氯化钙(或过量氯化钡溶液)溶液. | “猜想一”成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com