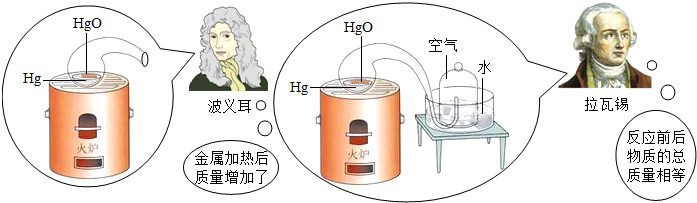
早在三百多年前,化学家们就对化学反应进行了定量研究.1673年,英国化学家波义尔在一只敞121的容器中加热金属,反应后他打开容器盖进行称量,结果发现反应后的质量增加了.这一实验导致波义尔没有发现质量守恒定律.
讨论:你能说说波义尔没有发现质量守恒定律的原因吗?______.
【答案】分析:金属汞铜放在密闭的容器里煅烧,消耗容器内的氧气生成了氧化铜,根据质量守恒定律,固体增加的质量即参加反应的氧气的质量.
解答:解:根据质量守恒定律得:研究反应前后质量关系的实验必须要将所有反应物和所有生成物的质量算入,在波义尔所做的实验中,由于反应后打开容器盖进行称量,导致外界空气进入容器中,从而使质量变大,因此他没有发现这一定律.
故答案为:因为研究反应前后质量关系的实验必须要将所有反应物和所有生成物的质量算入,在波义尔所做的实验中,由于反应后打开容器盖进行称量,导致外界空气进入容器中,从而使质量变大,因此他没有发现这一定律.
点评:根据反应只有氧气一种气体参加的特点,利用质量守恒定律,由反应前后固体质量变化确定参加反应氧气的质量是进行计算的基础.