
配制一定质量分数氯化钠溶液的一些操作步骤见下图.正确的操作顺序是
[
]
|
A .④⑤①②③ |
B .①②③④⑤ |
|
C .③④①②⑤ |
D .②①④③⑤ |
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
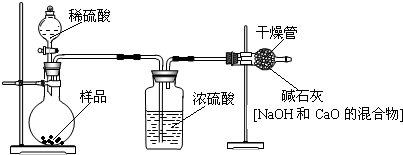
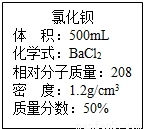
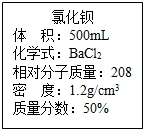 实验室有一瓶浓氯化钡溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题.我市某中学课外活动小组在测定RCl和R2S04形成混合物的百分组成时(R代表某金属元素).进行了以下实验.
实验室有一瓶浓氯化钡溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题.我市某中学课外活动小组在测定RCl和R2S04形成混合物的百分组成时(R代表某金属元素).进行了以下实验.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
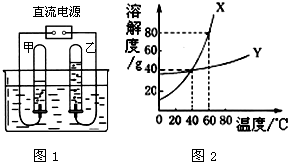 水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:
水是重要的自然资源,在进行化学实验和溶液中都需要水.请按要求回答下列问题:| 感官指标 | 化学指标 | 细菌指标 |
| 水质无色无味澄清 | PH:6.5~8.5 | 细菌总个数<100个/mL等 |
查看答案和解析>>
科目:初中化学 来源:2010年黑龙江省哈尔滨市中考化学模拟试卷(三)(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com