
| A. | 锌 | B. | 铜 | C. | 铝 | D. | 银 |
分析 铜、银在金属活动性顺序中,排在氢的后面,不能和稀硫酸反应;根据化学方程式计算,可以判断混合物的组成.
解答 解:设5.6g铁与足量的稀硫酸充分反应生成氢气的质量为X,
Fe+H2SO4═FeSO4+H2↑
56 2
5.6g X
$\frac{56}{2}=\frac{5.6g}{X}$ 解得:X=0.2g;
设5.6g锌与足量的稀硫酸充分反应生成氢气的质量为Y,
Zn+H2SO4═ZnSO4+H2↑
65 2
5.6g Y
$\frac{65}{2}=\frac{5.6g}{Y}$ 解得:Y=0.17g,
设5.6g铝与足量的稀硫酸充分反应生成氢气的质量为Z,
2Al+3H2SO4═Al2(SO4)+3H2↑
54 6
5.6g Z
$\frac{54}{6}=\frac{5.6g}{Z}$ 解得:Z=0.62g,
由此可知,铜、银不与硫酸反应,如混有铜或银,生成的气体小于0.2g.不纯的铁5.6g中,如果含有锌,则生成的氢气小于0.2g,如果含有铝,则生成的氢气大于0.2g,所以C符合题意.
故选:C.
点评 解答本题要注意临界点,即以5.6g为纯铁时为基础,计算出生成氢气的质量,然后再通过计算判断出杂质是什么物质.


科目:初中化学 来源: 题型:解答题
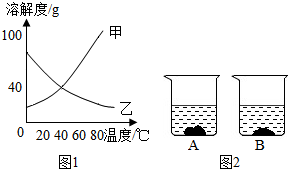
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
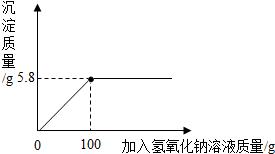 某氯化镁样品中含有少量的不溶于水也不和其它物质反应的杂质,某同学取此样品10g,加入 130.3g的水使其完全溶解,然后逐滴的向其中加入一定浓度的氢氧化钠溶液,生成沉淀的质量与所加氢氧化钠溶液的关系如图所示:
某氯化镁样品中含有少量的不溶于水也不和其它物质反应的杂质,某同学取此样品10g,加入 130.3g的水使其完全溶解,然后逐滴的向其中加入一定浓度的氢氧化钠溶液,生成沉淀的质量与所加氢氧化钠溶液的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
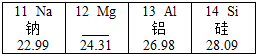 如图是元素周期表的一部分.原子序数为12的元素名称为镁;等质量的钠和铝,所含原子数较多的是钠(或Na);已知SiO2与CO2具有相似的化学性质,则二氧化硅与氢氧化钠溶液反应的化学方程式为2NaOH+SO2=Na2SiO3+H2O.
如图是元素周期表的一部分.原子序数为12的元素名称为镁;等质量的钠和铝,所含原子数较多的是钠(或Na);已知SiO2与CO2具有相似的化学性质,则二氧化硅与氢氧化钠溶液反应的化学方程式为2NaOH+SO2=Na2SiO3+H2O.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| OH- | NO3- | Cl- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
| 实验步骤 | 实验操作 | 实验现象 | 实验结论或化学方程式 |
| 步 骤 一 | 取样品,加水配制成溶液,并向其中滴加适量氯化钙溶液,充分反应后过滤 | 有白色沉淀生成 | 氢氧化钠已变质.写出加入氯化钙溶液后发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl. |
| 步 骤 二 | 取上述少量滤液于试管中,滴加无色酚酞溶液 | 酚酞溶液变 为红 色 | 氢氧化钠部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 溶剂 | 乙醇 | |
| 溶质 | 氢氧化钠 | 碳酸钠 |
| 溶解性 | 易溶 | 难溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 牛奶 红烧肉 | B. | 米饭 鸡蛋 | C. | 精肉 面条 | D. | 水果 蔬菜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com