
 地铁是哈尔滨市市民绿色出行的一种方式.哈尔滨市地铁1号线车型确定为B型车,B 型车通常釆用 铝合金和不锈钢车体,车辆内一般不使用木材.下列有关铝合金和不锈钢的说法错误的是( )
地铁是哈尔滨市市民绿色出行的一种方式.哈尔滨市地铁1号线车型确定为B型车,B 型车通常釆用 铝合金和不锈钢车体,车辆内一般不使用木材.下列有关铝合金和不锈钢的说法错误的是( )| A. | 不锈钢的硬度比铁的硬度大 | |
| B. | 铝合金和不锈钢具有很好的抗腐蚀性能 | |
| C. | 不锈钢和铝合金均属于合成材料 | |
| D. | 不锈钢除含碳外还含有少量的铬和镍 |
分析 合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质.合金概念有三个特点:①一定是混合物;②合金中各成分都是以单质形式存在;③合金中至少有一种金属.合金的性质是:合金的硬度大,熔点低,耐腐蚀;因此不锈钢的硬度比铁的硬度大,铝合金的熔点比铝的熔点低;铝合金和不锈钢具有很好的抗腐蚀性能.金属材料包括纯金属和合金,因此铝合金和不锈钢都属于金属材料;不锈钢是铁的合金,不锈钢除含碳外还含有少量的铬、镍等.
解答 解:A、合金的硬度大,熔点低,耐腐蚀,因此不锈钢的硬度比铁的硬度大,正确但不符合题意,故选项错误;
B、合金的硬度大,熔点低,耐腐蚀,铝合金和不锈钢具有很好的抗腐蚀性能,正确但不符合题意,故选项错误;
C、金属材料包括纯金属和合金,因此铝合金和不锈钢都属于金属材料,不是合成材料,错误符合题意,故选项正确;
D、不锈钢是铁的合金,不锈钢除含碳外还含有少量的铬、镍等,正确但不符合题意,故选项错误;
故选C
点评 本题主要考查合金与合金的性质,合金概念的三个特点要记牢;还要理解合金的性质,即合金的硬度大,熔点低,耐腐蚀.本考点基础性强,比较好把握.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 猜想 | 方案 | 证据 | 结论 |
| 氯化钡可能已完全反应 | 取少量滤液,加入稀硫酸溶液,观察现象 | 无白色沉淀生成 | 氯化钡已完全反应 |
| 硫酸钠可能已完全反应 | 取少量滤液,加入氯化钡溶液,观察现象 | 有白色沉淀生成 | 硫酸钠未完全反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
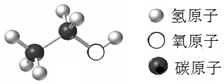
| A. | 乙醇分子是由三种元素组成的化合物 | |
| B. | 一个乙醇分子中含有28个质子 | |
| C. | 乙醇中碳、氧元素的质量比为3:2 | |
| D. | 乙醇分子是由中2个碳原子、6个氢原子、1个氧原子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| B. | 向氢氧化钠溶液中滴入硫酸铜溶液产生红褐色沉淀 | |
| C. | 木炭在氧气中燃烧产生浓厚的白烟 | |
| D. | 铁在氧气中剧烈燃烧,生成白色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
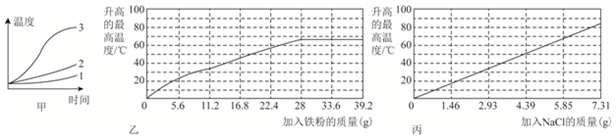
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com