
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 166.5 | 166.3 | 166.1 | 166.1 |
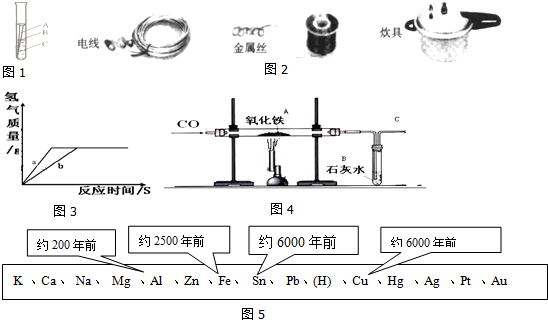
分析 (1)根据铁生锈的条件,分析防锈方法;
(2)根据金属的用途与性质之间的关系解答.
(3)分析铝在空气中所发生的变化,解释虽然铝的活动性比铁强,但却表现出良好的抗腐蚀性的原因;
(4)利用图中数据,对比大规模开发、利用的与金属其它因素间的关系,判断与金属大规模开发、利用的先后顺序有关的因素.
(5)由已知:“用质量相等的镁粉和铝粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应”,若酸完全反应,金属都剩余,则生成氢气相等,若金属完全反应,则生成氢气一定不相等.
(6)回顾一氧化碳还原氯化铁的实验,回答对该实验的操作所提出的问题.根据铁的金属活动性比氢强,能与稀盐酸反应,设计实验方案;
(7)由表中的实验数据可判断第四次称量时已完全反应,利用质量守恒定律,可计算放出氢气的质量;
根据化学方程式求出铁的质量,进而求出生铁中铁质量分数.
解答 解:(1)铁生锈的过程是铁与氧气、水蒸气发生化学反应,所以与水面接触的地方易生锈,因此可以通过刷油漆的方法防止生锈.
(2)金属能做成导线是因为有导电性,抽成丝是因为有延展性,做成锅是因为导热性.
(3)铝在空气中与氧气化合,在铝的表面生成致密的氧化铝薄膜(或氧化铝膜),阻止了铝进一步与氧气的接触;
(4)由图示信息可得到,金属大规模开发、利用的先后顺序跟③金属的活动性、⑤金属冶炼的难易程度相关,活动性强的金属冶炼难度大,使用则较晚;
(5)根据化学方程式:Mg+2HCl=MgCl2+H2↑;2Al+6HCl═2AlCl3+3H2↑进行计算:
A、因为镁的活动性比铝的活动性强,镁反应速度快,故A说法正确;
B、如果盐酸均反应完,镁恰好完全反应,铝有剩余,故B说法正确;
C、如果镁、铝都反应完,则产生的氢气一定不等,说法不正确.
D、盐酸均反应完,镁、铝都反应完,生成的氢气一定相等,故D说法正确;
故选AB;
(6)一氧化碳还原氧化铁生成铁和二氧化碳,故看到的现象为固体由红变黑,澄清石灰水变浑浊,为防止生成的铁被氧化,实验结束前还要继续通一氧化碳直到冷却,故不需要断开,铁的金属活动性比氢强,能与稀盐酸反应生成氯化亚铁和氢气,可用小试管取待测样品少量,加入适量的稀盐酸,观察到有气泡产生,溶液变为浅绿色,说明生成的固体是铁.
(7)反应前总质量一反应后总质量=生成氢气的质量,反应完毕后总质量为166.1g,所以氢气质量=11.5+100g+55g-166.1g=0.4g
解:设铁的质量为x
Fe+H2SO4 =FeSO4 +H2↑;
56 2
x 0.4g
$\frac{56}{2}=\frac{x}{0.4g}$
x=11.2g
生铁中铁的质量分数为:$\frac{11.2g}{11.5g}×100$%=97.4%
故答案为(1)B;涂油;
(2)良好导电性(或导热性等);
(3)4Al+3O2═2Al2O3;
(4)A; (5)AB_;
(6)①固体变黑、澄清石灰水变浑浊;②不需要.
③实验操作:用小试管取待测样品少量,加入适量的稀盐酸
实验现象:有气泡产生,溶液变为浅绿色
实验结论:一氧化碳还原氧化铁生成的固体是铁
(7)①0.4;
②97.4%.
点评 本题通过一氧化碳还原氧化铁的化学反应让同学们了解炼铁的原理,通过对反应前后物质的变化来判断现象以及对最后的环境污染物进行处理,是同学们应掌握的基本技能.注意:用CO、H2还原氧化铜时应注意操作的先后顺序:应先通气体,以便把装置中的空气赶净,然后再给试管加热.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③④ | C. | ②④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀硫酸的体积/mL | 20 | 20 | 20 | 20 |
| 残留金属的质量/克 | 21.75 | 18.5 | 15.25 | 15.25 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com