
分析 根据题干提供的信息结合分离混合物的方法、化学方程式的书写、以及根据溶液的计算的知识进行分析解答即可.
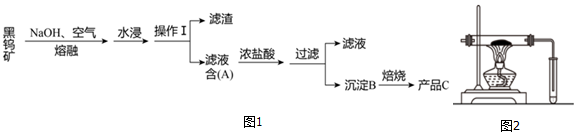
解答 解:(1)操作1得到的是滤渣和滤液,故是过滤操作,熔融FeWO4、MnWO4和氢氧化钠反应生成氢氧化铁、氢氧化锰和钨酸钠,氢氧化铁和氢氧化锰不溶于水,钨酸钠易溶于水,经过水浸、过滤,A为钨酸钠;故填:过滤;Na2WO4;
(2)钨酸钠和浓盐酸反应生成钨酸和氯化钠,化学方程式为:Na2WO4 +2HCl═H2WO4↓+2NaCl;故填:Na2WO4 +2HCl═H2WO4↓+2NaCl;
(3)钨酸高温生成氧化钨,一氧化碳还原氧化钨生成钨和二氧化碳,化学方程式为:WO3 +3CO$\frac{\underline{\;\;△\;\;}}{\;}$W+3CO2;由于一氧化碳是可燃性气体,不纯时加热可能会产生爆炸,故操作中应注意先通一氧化碳后加热,一氧化碳是有毒的气体,需要进行尾气处理,故填:WO3 +3CO$\frac{\underline{\;\;△\;\;}}{\;}$W+3CO2;排尽装置内的空气,防止加热时爆炸;没有尾气处理;
(4)设需要50%的氢氧化钠溶液的质量为x,则有:50%x=100kg×20%,x=40kg,故填:40;
(5)氢氧化钠与硫酸铵反应生成硫酸钠、氨气和水,故填:(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑.
点评 本题主要考查学生常见金属的冶炼知识,并考查正确书写化学方程式的能力,需要学生在平时多加练习.


科目:初中化学 来源: 题型:选择题
| A. | Cu | B. | Fe2O3 | C. | Mg | D. | CuO |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 氯化钠溶解度(克) | 35.8 | 36.0 | 36.3 | 36.4 | 37.0 | 37.3 | 37.8 |
| 硝酸钾溶解度(克) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 制取氢氧化铁 | B. | 制取铜 | C. | 制取氢气 | D. | 制取碳酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用洗洁精清洗油污的餐具 | B. | 用自来水洗手 | ||
| C. | 用汽油洗去衣服上的油污 | D. | 用盐酸清除试管内壁附着的碳酸钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
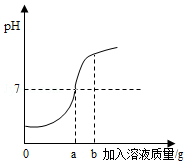 用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示:
用质量分数为5%的稀盐酸和10%的氢氧化钠溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com