
 铝是目前人们在生产、生活中使用较多的一种金属.
铝是目前人们在生产、生活中使用较多的一种金属.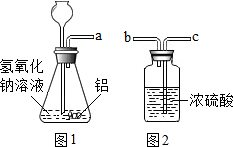
分析 (1)
A、根据原子的结构示意图的意义解答;
B、根据氧元素是地壳中含量最多的元素解答;
C、根据由该元素的原子结构示意图可知,最外层电子数是3,小于4,该元素的原子容易失去电子解答;
D、根据由该元素的原子结构示意图可知,最外层电子数是3,小于4,该元素的原子容易失去电子解答;
(2)【提出猜想】根据质量守恒定律,化学反应前后元素的种类不变解答;
【进行实验】①根据氧气能够支持燃烧解答;
②根据浓硫酸干燥气体是从长管进解答;
【得出结论】根据铝、氢氧化钠和水反应生成氢气和偏铝酸钠(NaAlO2),写出反应的化学方程式解答;
【交流讨论】根据氢气具有可燃性,点燃时易发生爆炸解答;
【反思提升】根据研究成果分析解答.
(3)根据氢气的质量利用反应的化学方程式解答.
解答 解:
(1)
A、据铝原子的结构示意图可知:铝原子的相质子数为13,无法确定相对原子质量,故错误;
B、氧元素是地壳中含量最多的元素,铝位于第二,故错误;
C、由该元素的原子结构示意图可知,最外层电子数是3,小于4,该元素的原子容易失去电子,故正确;
D、由该元素的原子结构示意图可知,最外层电子数是3,小于4,该元素的原子容易失去电子,形成阳离子,铝元素在化合物中的化合价为+3价,故正确.
(2):【提出猜想】根据质量守恒定律,化学反应前后元素的种类不变,反应前无碳元素,反应后也无碳元素,故小雨猜想是错误的;
【进行实验】①氧气能够支持燃烧,反应一段时间后,将带火星的木条放在a处,观察到带火星的木条不复燃,则她的猜想是错误的.
②浓硫酸干燥气体是从长管进,用图Ⅱ所示装置干燥从a导管出来的气体,将管口a与c端管口连接;
【得出结论】铝、氢氧化钠和水反应生成氢气和偏铝酸钠(NaAlO2),反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
【交流讨论】氢气具有可燃性,点燃时易发生爆炸;
【反思提升】根据研究成果可知:有两项是通过对异常现象研究得出的.它们是波义耳不慎将浓盐酸见到花瓣上从而发现了酸碱指示剂,拉瓦锡深入研究前人忽视的异常现象发现了氧气;
(3)所需氢氧化钠的质量为x
2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
80 6
x 1.2g
$\frac{80}{x}=\frac{6}{1.2g}$
x=16g
则所需氢氧化钠溶液的质量分数是:$\frac{16g}{40g}×$100%=40%.
故答案为:
(1)D;
(2)【提出猜想】化学反应前后元素的种类不变,反应前无碳元素,反应后也无碳元素;
【进行实验】①带火星的木条不复燃;②c;
【得出结论】2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
【交流讨论】氢气具有可燃性,点燃时易发生爆炸;
【反思提升】AC.
(3)则所需氢氧化钠溶液的质量分数是40%.
点评 题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
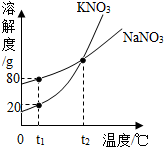 如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )
如图表示是KNO3和NaNO3的溶解度曲线.下列说法正确的是( )| A. | t1℃时,两种溶液中溶质质量分数一定不相等 | |
| B. | t1℃时,在50g水里加入15g KNO3固体,充分溶解,得到60g溶液 | |
| C. | t1℃时,硝酸钾、硝酸钠两物质饱和溶液升温到t2℃后,溶质质量分数相等 | |
| D. | 两种饱和溶液从t2℃降温到t1℃时,析出晶体:硝酸钾一定多于硝酸钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用酚酞鉴别食盐水和稀醋酸 | |
| B. | 用胆矾检验汽油中是否掺水 | |
| C. | 用燃着的木条检验某气体是否是二氧化碳 | |
| D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
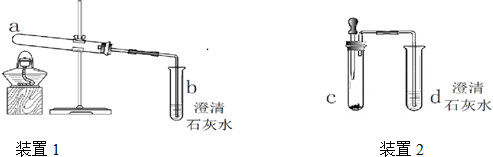
| 序号 | 实验方案 | 实验现象 | 实验结论 |
| Ⅰ | 在装置1的a试管中放入小苏打,加热 | a试管口内壁有无色液滴,石灰水变浑浊. | b试管中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O. 猜想1正确 |
| Ⅱ | 在装置1的a试管中放入酒石酸氢钾,加热 | a试管口内壁有无色液滴,石灰水不变浑浊 | 猜想2不正确 |
| Ⅲ | 在装置2的c试管中放入小苏打和酒石酸氢钾的混合物,滴加水. | c试管中有气泡产生, 石灰水变浑浊 | 猜想3正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
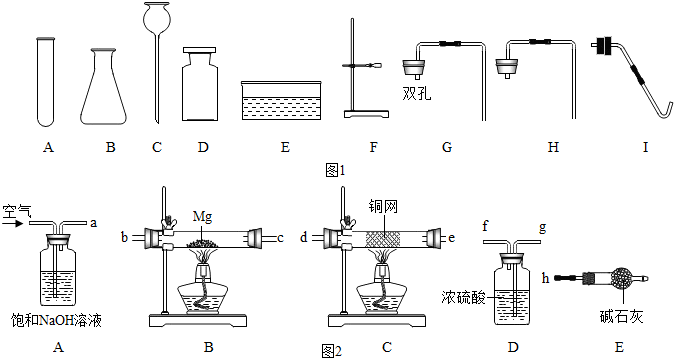
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | “洁厕灵”可用于清洁大理石地面 | |
| B. | “洁厕灵”和“84消毒液”两者混合使用,可以增强清洁能力 | |
| C. | “84消毒液”中NaClO属于盐,其中C1元素的化合价呈+1价 | |
| D. | “洁厕灵”与“84消毒液”混合后发生置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
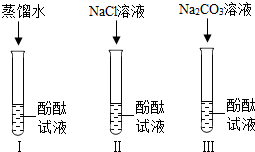 实验小组同学在实验中发现Na2CO3溶液能使酚酞试液变红色.于是他们进行了以下实验探究:
实验小组同学在实验中发现Na2CO3溶液能使酚酞试液变红色.于是他们进行了以下实验探究:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com