人类每时每刻都离不开空气,没有空气就没有生命,也就没有生机勃勃的地球.
(1)空气主要由
氮气
氮气
(填物质名称)和氧气组成,此外,还含有少量的稀有气体等.
(2)空气中的各种成分广泛应用于多个领域,其中氧气可用于
B
B
(填字母序号,下同),稀有气体可用于
A
A
.
A.制造霓虹灯 B.医疗急救
(3)为了保护空气,在我国新颁布的《环境空气质量标准》中,基本监控项目增设了PM2.5浓度限值,与该项目监测项目有关的是
D
D
(填字母序号).
A.二氧化硫 B.二氧化氮 C.一氧化碳 D.可吸入颗粒物
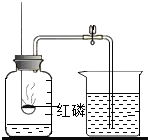
(4)右图所示的装置可用于测定空气中氧气的含量.
①请补全下列实验步骤.
a.按图示连接好装置;
b.
检查装置气密性
检查装置气密性
;
c.在集气瓶内加入少量水,并将水面上方空间分为五等分,用弹簧夹夹紧胶皮管;
d.取足量红磷放入燃烧匙中,点燃后立即伸入瓶中,并把塞子塞紧;.
e.待红磷熄灭并冷却至室温后,打开弹簧夹.
②红磷燃烧的现象是
产生大量白烟,放热
产生大量白烟,放热
,反应的文字表达式为
.
③冷却至室温后打开弹簧夹,水能进入集气瓶中的原因是
磷与氧气反应生成固体五氧化二磷,瓶内氧气被消耗,压强降低,冷却后打开弹簧夹,水被
吸入集气瓶中
磷与氧气反应生成固体五氧化二磷,瓶内氧气被消耗,压强降低,冷却后打开弹簧夹,水被
吸入集气瓶中
.
④若某同学在实验后得出结论:空气中氧气的体积约占
.能得出此结论的实验现象为
进入集气瓶中的水的体积约占瓶内水面上方空间的五分之一
进入集气瓶中的水的体积约占瓶内水面上方空间的五分之一
.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案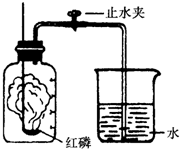 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: 人类每时每刻都离不开空气,没有空气就没有生命,也就没有生机勃勃的地球.
人类每时每刻都离不开空气,没有空气就没有生命,也就没有生机勃勃的地球. 测定空气中氧气含量的方法很多,图1所示的是用红磷在空气中燃烧的测定方法.实验过程是:
测定空气中氧气含量的方法很多,图1所示的是用红磷在空气中燃烧的测定方法.实验过程是:
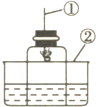 如图所示,用此类装置测量空气中氧气的含量.在燃烧匙中加入红磷,红磷与空气中的氧气发生化学反应生成五氧化二磷固体,请按要求填空.
如图所示,用此类装置测量空气中氧气的含量.在燃烧匙中加入红磷,红磷与空气中的氧气发生化学反应生成五氧化二磷固体,请按要求填空.