
 如图有一空心铜球悬浮在硫酸铜溶液中,且铜球不与烧杯内壁和底部接触,现向硫酸铜溶液中投入一小块铁,待铁块充分反应后(忽略溶液体积的变化),下列对铜球静止后的有关判断正确的是( )
如图有一空心铜球悬浮在硫酸铜溶液中,且铜球不与烧杯内壁和底部接触,现向硫酸铜溶液中投入一小块铁,待铁块充分反应后(忽略溶液体积的变化),下列对铜球静止后的有关判断正确的是( )| A. | 漂浮 | B. | 浮力不变 | C. | 浮力变大 | D. | 沉到底部 |
科目:初中化学 来源:【全国区级联考】江苏省盐城市亭湖区2017届九年级毕业班下学期第二次质量检测化学试卷 题型:选择填充题
下列有关物质分类或归类正确的是
A. 氧化物:生石灰和熟石灰 B. 复合肥: 硝酸钾和碳酸钾
C. 硬水:蒸馏水和矿泉水 D. 碳单质:金刚石和石墨
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
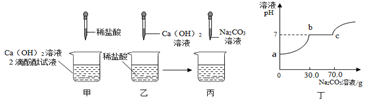
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | NaOH溶液 | B. | CuSO4溶液 | C. | K2SO4溶液 | D. | Na2CO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
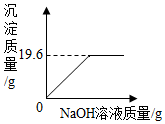 有一包固体粉末,由CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或几种组成,某实验小组对其组成成分进行了以下探究活动.
有一包固体粉末,由CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或几种组成,某实验小组对其组成成分进行了以下探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源:【全国市级联考】重庆市2017届九年级中考模拟(B)化学试卷 题型:推断题
下图中每条直线两端的物质在一定条件下都可以发生化学反应。其中甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、盐酸四种物质中的一种。
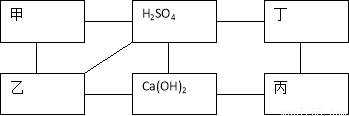
(1)写出甲和乙两种物质的化学式:甲 、乙 ;
(2)写出下列物质发生反应的化学方程式:
乙和Ca(OH)2: ;
丙和丁: ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com