
分析 (1)根据碳酸氢铵受热易分解分析;
(2)根据复分解反应发生的条件以及书写方程式的方法来分析;
(3)根据实验现象来分析解答;
(4)根据化学反应前后的元素种类与质量的守恒来分析.
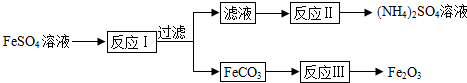
解答 解:(1)NH4HCO3受热易分解,为了减少NH4HCO3溶液的减少,应控制温度在35℃以下,故填:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑;
(2)反应Ⅱ是复分解反应,由流程图分析可知是稀硫酸与反应Ⅰ中过量的NH4HCO3反应,生成硫酸铵、水和二氧化碳,故填:2NH4HCO3+H2SO4═(NH4)2SO4+2H2O+2CO2↑;
(3)红褐色固体是Fe(OH)3,FeCO3、H2O和O2反应生成Fe(OH)3和CO2;故填:O2、H2O;
(4)解:设Fe2O3的质量为x,根据化学反应前后铁元素质量不变可得:$\frac{112}{160}$×100%×x+$\frac{56}{72}$×100%×(15.84 kg-x)=$\frac{56}{116}$×100%×23.2 kg,解答x=14.4 kg.故填:14.4.
点评 本题属于信息题的考查,考查了铁及其化合物的性质,主要通过发生流程知道反应物和生成物进行相关问题的分析,能够考查学生的知识分析能力.


 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
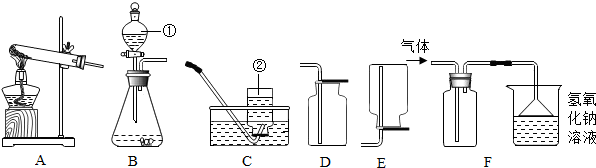
| A. | 仅需水 | B. | 仅需氧气 | C. | 水或氧气 | D. | 水和氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
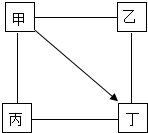 甲、乙、丙、丁是初中化学常见的物质,常温下,它们具有如图所示关系.“-”表示连接的两种物质能反应,“→”表示物质转化的方向,下列推断错误的是( )
甲、乙、丙、丁是初中化学常见的物质,常温下,它们具有如图所示关系.“-”表示连接的两种物质能反应,“→”表示物质转化的方向,下列推断错误的是( )| A. | 若甲是HCl,则丁可能是CaCl2 | |
| B. | 若甲是HCl,则乙和丙中可能有一个为碱 | |
| C. | 若甲是Ca(OH)2,则丁可能是NaOH | |
| D. | 若甲是Ca(OH)2,则乙和丙中至少有一个为酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 合成纤维、合金、合成橡胶都是有机合成材料 | |
| B. | 喝牛奶、豆浆等富含蛋白质的食品可有效缓解重金属盐中毒现象 | |
| C. | 缺碘易患龋齿 | |
| D. | 大量使用天然气作燃料符合“低碳生活”理念 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
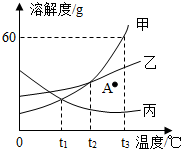 如图为甲、乙、丙三种物质的溶解度曲线.
如图为甲、乙、丙三种物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量的熟石灰样品于烧杯中,加适量的水充分溶解后过滤. 向滤液中加入适量的酚酞(3)不用填溶液; | 溶液变为红色(4)不用填; | 乙的猜想不正确 |
| 向滤出固体中加入适量稀盐酸(5)不用填溶液. | 固体溶解,有气泡产生(6)不用填. | 你的猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
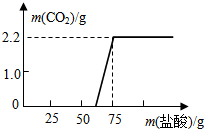 某学校科学兴趣小组为了探究实验室中久置的NaOH的变质程度,具体如下:
某学校科学兴趣小组为了探究实验室中久置的NaOH的变质程度,具体如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com