
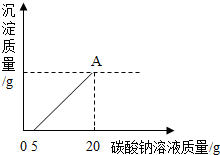
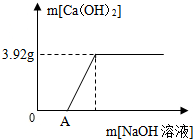
 为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:
为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:分析 (1)加入的5g碳酸钠溶液和稀盐酸反应生成氯化钠、水和二氧化碳;
(2)加入的15g碳酸钠溶液和氯化钙反应生成碳酸钙沉淀和氯化钠,根据提供的数据可以计算A点处溶液中溶质的质量.
解答 解:(1)加入的碳酸钠溶液和稀盐酸、氯化钙反应,说明原废液中的溶质成分有HCl、CaCl2.
故填:HCl、CaCl2.
(2)设A点处溶液中溶质氯化钠的质量为x,
由Na2CO3+2HCl=2NaCl+H2O+CO2↑,Na2CO3+CaCl2═CaCO3↓+2NaCl可知,Na2CO3~2NaCl,则:
Na2CO3 ~2NaCl,
106 117
20g×10.6% x
则$\frac{106}{117}=\frac{20g×10.6%}{x}$,解得x=2.34g,
设碳酸钠溶液与氯化钙反应生成碳酸钙的质量为a,
Na2CO3+CaCl2=CaCO3↓+2NaCl,
106 100
1.59g a
则$\frac{106}{100}=\frac{1.59g}{a}$,解得a=1.5g.
设碳酸钠和稀盐酸反应生成二氧化碳的质量为z,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
5g×10.6% z
则$\frac{106}{5g×10.6%}=\frac{44}{z}$,解得z=0.22g,
A点处溶液中溶质的质量分数为:$\frac{2.34g}{20g+20g-1.5g-0.22g}×100%$=6.1%.
故答案为:
(1)HCl和CaCl2,(2)6.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰用于人工降雨 | |
| B. | 小苏打用于烘焙糕点 | |
| C. | 用氢氧化钠改良酸性土壤 | |
| D. | 用食醋除去水壶中的水垢[主要成分是CaCO3和Mg(OH)2] |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
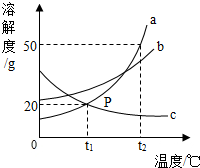 如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线,下列说法错误的是( )| A. | P点表示t1℃时,a、c两种物质的饱和溶液溶质质量分数相等 | |
| B. | t2℃时a、b、c三种物质的溶解度由大到小的顺序是a>b>c | |
| C. | t2℃时,将30g a物质加入到50g水中充分搅拌,得到80g a的饱和溶液 | |
| D. | 将接近饱和的c溶液变为饱和溶液,除采用加溶质、蒸发溶剂外,还可采用升温的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
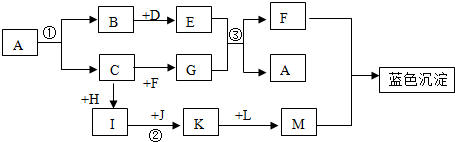
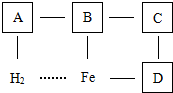 已知ABCD分别为H2SO4、NaOH、CuCl2和CuO中的一种.它们之间的关系如图所示(“--”表示能反应,“…”表示不能反应):
已知ABCD分别为H2SO4、NaOH、CuCl2和CuO中的一种.它们之间的关系如图所示(“--”表示能反应,“…”表示不能反应):查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
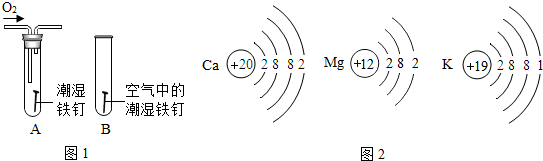
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳:用于灭火 | B. | 明矾:用于净水 | ||
| C. | 烧碱:用于食用碱 | D. | 氯化钠:用于配制生理盐水 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某环保小组监测到一工厂向河水中排放的酸性废液中含有CuSO4.
某环保小组监测到一工厂向河水中排放的酸性废液中含有CuSO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com