
����Ŀ���������ҽ����������ɵĻ�����(��Ҫ�ɷ���FeS2)��������H2SO4����Ҫԭ�ϣ����û���������H2SO4�ĵ�һ����ӦΪ��4FeS2+11O2�T2Fe2O3+8X�����ò���Fe2O3��ұ��������Ҫԭ�ϣ��ش��������⣺
(1)��֪FeS2��Fe�Ļ��ϼ�Ϊ+2����S�Ļ��ϼ�Ϊ________��
(2)X�Ļ�ѧʽ��_________��
(3)д����¯��Fe2O3ת�������Ļ�ѧ����ʽ__________________________��
���𰸡� ��1 SO2 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
����������1��FeS2����Ϊ������������Ԫ����+2�ۣ�����Ԫ�صĻ��ϼ�Ϊx�����ݻ�������Ԫ���������ϼ۵Ĵ�����Ϊ0����ô��+2��+2x=0��x=��1����2���������غ㶨�ɣ���Ӧǰ��ԭ�����ࡢ��Ŀ�����䣬�ɷ�Ӧ�Ļ�ѧ����ʽ4FeS2+11O2![]() 2Fe2O3+8X����Ӧǰ��������ԭ�Ӹ����ֱ�Ϊ4��8��22����Ӧ�������������������ԭ�Ӹ����ֱ�Ϊ4��0��6�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��8X�����к���8����ԭ�Ӻ�16����ԭ�ӣ���ÿ��X������1����ԭ�Ӻ�2����ԭ�ӹ��ɣ�������X�Ļ�ѧʽΪSO2����3��һ����̼����������Ӧ�������Ͷ�����̼�����Կ�������ұ��ԭ�ϣ���Ӧ����һ����̼���������������������Ͷ�����̼����Ӧ�����Ǹ��£����Է���ʽ�ǣ�3CO+Fe2O3
2Fe2O3+8X����Ӧǰ��������ԭ�Ӹ����ֱ�Ϊ4��8��22����Ӧ�������������������ԭ�Ӹ����ֱ�Ϊ4��0��6�����ݷ�Ӧǰ��ԭ�����ࡢ��Ŀ���䣬��8X�����к���8����ԭ�Ӻ�16����ԭ�ӣ���ÿ��X������1����ԭ�Ӻ�2����ԭ�ӹ��ɣ�������X�Ļ�ѧʽΪSO2����3��һ����̼����������Ӧ�������Ͷ�����̼�����Կ�������ұ��ԭ�ϣ���Ӧ����һ����̼���������������������Ͷ�����̼����Ӧ�����Ǹ��£����Է���ʽ�ǣ�3CO+Fe2O3![]() 2Fe+3CO2��
2Fe+3CO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������������������Ϊ10%����������Һ����ˮ�ĵ��ʵ��
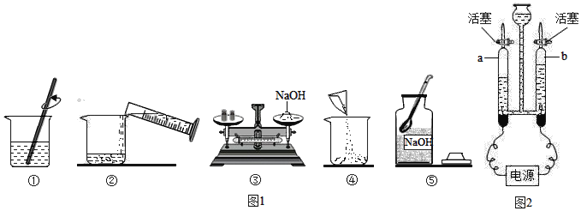
ʵ��һ��ʵ��������50����������Ϊ10%������������Һ����ͼ1��С��ʵ���������ʾ��ͼ��
(1)ͼ1��һ�����Դ���IJ�����_____(�����)������������������ͼʾ����ű�ʾ������Һ����ȷ����˳��_____��
(2)ͼ1���в����������Ŀ����_____��
(3)����ʱ���������ƹ���Ӧ������ƽ_____(����������������)�̵��ձ��ڣ���ȡ�����ˮ(ˮ���ܶ�Ϊ1g/cm3)��Ӧѡ�����Ͳ�Ĺ����_____mL(ѡ����10������100������250��)��
(4)���������Ƶ�����������Һ��������������С��10%�����¸ý������ԭ����_____(�����)
������Ͳ��ȡˮʱ���Ӷ��� ��������Һ���ձ�����������ˮ��ϴ
���������ƹ��岻�� ��ʢװ��Һ���Լ�ƿ������ˮ��ϴ
ʵ�����ˮ�ĵ��ʵ��
����ͼװ�ý���ˮ�ĵ��ʵ�飬��֪����������ˮ�ĵ��ʵ���У�ֻ����ǿˮ�ĵ���������
(5)��ʼ��Ӧǰa��b�����ڶ�������Һ���رջ�������ͨ��Դ��һ��ʱ������ܲ�����������ͼ2��ʾ����a���·�����Ӧ�ӵ�Դ��_____��(����������������)����_____��֤b���е����壬д�����ˮ�Ļ�ѧ��Ӧʽ��_____���÷�Ӧ�Ļ�����Ӧ����Ϊ_____
(6)˵��ˮ��һ�ֻ������ʵ����ʵ��_____��
(7)������Һ��������������_____10%(������������=����������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ȷ��ӳ���Ӧ�����и����仯��ϵ���ǣ� ��
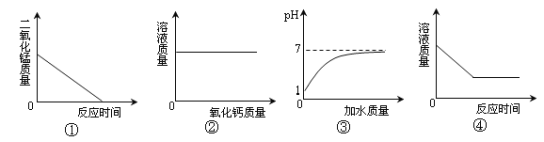
A��ͼ���Ǹ�����غͶ������̵Ļ�������
B��ͼ������һ���¶��µı�������������Һ�в��ϼ��������ƹ���
C��ͼ������pH��1������Һ�в��ϼ�ˮ
D��ͼ������һ��������ϡ�����м���п��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͭ����������ʹ�����硢Ӧ�ù㷺�Ľ�����
(һ)�ԹŴ���Ʒ����ʶ
��ͭ������˿��֯Ʒ���մ��������ҹ��Ŵ��Ͷ�������ĻԻͳɾͣ�
(1)������Ʒ���漰���IJ�����______(ѡ�����)��
A���������� B�����ǽ������� C�����ϲ���
(2)��ͼ1Ϊ��������Ŵ���ͭ��������̤���������������ܱ��������ԭ�������_____(ѡ�����)��
A��ͭ�Ļ������� B��ͭ�������� C�������ڵ��£���������
(��)����ͭ��ұ��
���ҹ��Ŵ����ÿ�ȸʯ��ͭ���漰��Ҫ��Ӧ�Ļ�ѧ����ʽ��_________��2CuO+C![]() 2Cu+CO2����
2Cu+CO2����
������ͭ��ʯ�г�����(Fe2O3)��������(Fe3O4)��������(FeS2)����ͭ��(CuFeS2)�ȣ�CuFeS2Ϊ��������ͭ������SԪ�صĻ��ϼ�Ϊ______��
(1)��ҵ���������ó����������Դ�����Ϊԭ��������Ӧ�Ļ�ѧ����ʽΪ______________��
���������û�����ͭ���ܵ�ԭ���ǣ�
�ٻ�����ͭ��������Եͣ���________________________________��
(2)�Ի�ͭ��Ϊԭ�ϣ�����������ͭ���ִ���ͭ���¹��գ�ԭ��Ϊ��4CuFeS2+17O2+2H2SO4![]() 4CuSO4+2Fe2(SO4)3+2H2O��
4CuSO4+2Fe2(SO4)3+2H2O��
��������Ӧ�����Һ�м���Fe�ۣ��õ�FeSO4��Һ��Cu��
�ٷ�����Ҫ��Ӧ�Ļ�ѧ����ʽ��Fe+Fe2(SO4)3=3FeSO4��________________________��
��FeSO4��Һ������Ũ����___________�����˵Ȳ����õ�FeSO47H2O���壮
(��)��ͭ��������ͭ�����IJⶨ
�ڿ�����Աָ���£���ȤС���ȡ25.00g��ͭ��(������Fe2O3��������������Ԫ�ص�����)ģ��������ͭ��ʹ��ȫ��ת��ΪCuSO4��Fe2(SO4)3��Һ������Һ�м������NaOH��Һ�õ�Cu(OH)2��Fe(OH)3���壮
(1)֤��NaOH��Һ�����ķ��������ã����ϲ���Һ�еμ�________��Һ��������
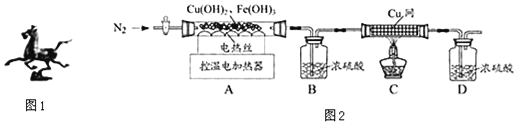
(2)��ͼ2װ�öԹ�������ȷֽ�ʵ�飮
�����ϡ�
����68��ʱ��Cu(OH)2�ֽ�ΪCuO����500��ʱ��Fe(OH)3�ֽ�ΪFe2O3��
����1400��ʱ��CuO�ֽ�ΪCu2O��O2��Fe2O3�ֽ�Ϊ���ӵ������������O2��
(1)װ���ʵ��װ�ú���Ҫ________________��
(2)ֹͣ���Ⱥ��������ͨN2���ɷ�ֹ������______________________________��
(3)���Ʋ�ͬ���¶ȶ�A�й�����ȣ����װ��B��C��ͭ���������仯�����
�¶�/�� | ���� | 100 | 550 | 1400 |
Bװ��/g | 200.00 | 201.80 | 205.04 | 205.04 |
C��ͭ��/g | 100.00 | 100.00 | 100.00 | 101.28 |
�ٴ˻�ͭ����ͭ����Ԫ�ص�������������(Cu)%=________����(Fe)%=__________��
�ڸ��ӵ����������ﻯѧʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
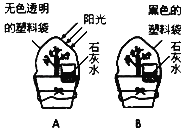
����Ŀ��̽����ֲ����������������õıȽ���ֲ�ﲻ�����й�����ã�Ҳͬʱ���к������ã�Ϊ�˱Ƚ϶��ߵIJ�ͬ���������������ʵ�飮��һ���ʵ��糿��ѡȡ��С���Ƶ�ͬ��ֲ�����裬�ڻ����ϸ�����һ�������ʯ��ˮ��Ȼ�������һ������ɫ�������ϴ���ס�����������£��� һ�����ú�ɫ���ϴ���ס������������(����ͼ)�������������ϴ��϶���һС�ڣ�������ȼ�ŵ�ľ�����飬����A��ľ����B�и�������A�е�ʯ��ˮ���ֳ��壬B�б���ǣ�
(1)A��ľ��ȼ�ո�����˵��A��_____���࣬�Ӷ�˵��������������ֲ����Ҫ����_____���ã�
(2)A��ʯ��ˮ���ֳ��壬��B�б���ǣ�˵��B��_____���࣬�Ӷ�˵����ȱ�ٹ��������£�ֲ����Ҫ����_____���ã�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��.Ϊ�ⶨijʯ��ʯ��Ʒ��̼��Ƶ�����������ijͬѧȡ30gʯ��ʯ��Ʒ����200gϡ������μ������У�ʵ���������£�
��һ�� | �ڶ��� | ������ | ���Ĵ� | |
ϡ��������/g | 50g | 50g | 50g | 50g |
���¹�������/g | 20g | 10g | 9g | 9g |
����(1)��ʯ��ʯ��Ʒ�Ĵ��ȡ�(2)200gϡ�����������Ȼ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾij��Ӧ����ʾ��ͼ��������![]() ����
���� ![]() ����
����![]() ���ֱ��ʾA��B��C���ֲ�ͬ�ķ��ӡ��÷�Ӧ�Ļ�ѧ����ʽ��A��B��C�Ļ�ѧ������֮��Ϊ
���ֱ��ʾA��B��C���ֲ�ͬ�ķ��ӡ��÷�Ӧ�Ļ�ѧ����ʽ��A��B��C�Ļ�ѧ������֮��Ϊ
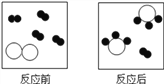
A. 4��3��1 B. 4��1��2 C. 3��1��3 D. 3��1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����ֻ�������壬û�к������� �� ��
A��H2 B��2H C��Fe D��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ѧϰ��ѧ֪ʶ�۲����������Ҫ�ӻ�ѧ�ӽǿ���ˮ��һ����Ҫ�����ʣ����ճ����������ʵ�������Ų�����������á��밴Ҫ��ش��������⣺
(1)����ɽǶȿ�����Ȼ������ʶ�����Ԫ����ɵģ�ˮ����__________________��ɵġ�
(2)�ӽṹ�Ƕȿ����������ʵĻ������з��ӡ�ԭ�ӡ����ӣ�ˮ����_____________���ɵġ�
(3)�ӱ仯�Ƕȿ����仯Ī���ˮ�����Ŵ���Ȼ�����档���ֱ仯�У����۽Ƕȿ������ֱ仯�ı���������__________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com