
【题目】根据下列装置回答问题。
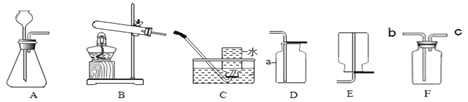
(1)请写标号仪器的名称:a______________。
(2)用高锰酸钾为原料制取较纯净的氧气可选用的装置组合为__________(填字母,下同),发生装置应作的改进是_____________,反应的化学方程式为_________________。
(3)实验室用锌粒和稀硫酸制取氢气,反应的化学方程式为__________________,可选用的发生装置是_______,若用F装置收集氢气,气体应从________端通入(填“b”或“C”)。
(4)已知:氨气极易溶与水,且与水反应生成氨水,氨气难溶于氢氧化钠溶液。
①碳酸氢铵是一种常用的氮肥,受热易分解,生成氨气、水、二氧化碳,该反应的化学方程式为__________。
②检验碳酸氢铵分解后的气体中含有二氧化碳,下列方案可行的是___________(填序号)。
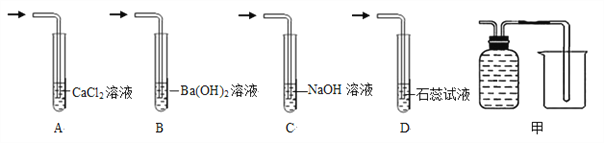
③甲图可用于分离碳酸氢铵分解产生的气体并回收氨气,广口瓶中应盛放的液体是_________,装置需要作怎样的改进才能达到实验目的?请用铅笔在答题卡相应位置画出。 _________________
【答案】 集气瓶 BC 在试管口放一团棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ Zn+H2SO4=ZnSO4+H2↑ A c NH4HCO3
K2MnO4+MnO2+O2↑ Zn+H2SO4=ZnSO4+H2↑ A c NH4HCO3![]() NH3↑+ H2O +CO2↑ B NaOH溶液
NH3↑+ H2O +CO2↑ B NaOH溶液 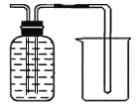
【解析】(1)集气瓶是收集气体的仪器;
(2)如果用高锰酸钾制氧气就需要加热,故选B装置,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;故高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,化学方程式为:2KMnO4 ![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,因此不需要加热;若用F装置收集氢气,气体应从短管进入,因为氢气密度比空气的密度小;反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(4)已知:氨气极易溶与水,且与水反应生成氨水,氨气难溶于氢氧化钠溶液。
①碳酸氢铵受热分解生成氨气、水、二氧化碳,化学方程式为:NH4HCO3 ![]() NH3 ↑+ H2O +CO2↑;
NH3 ↑+ H2O +CO2↑;
②检验二氧化碳,用澄清的石灰水,澄清的石灰水变浑浊,说明含有二氧化碳气体;
③分离碳酸氢铵分解产生的气体并回收氨气,可以将产生的气体通入氢氧化钠溶液,除去二氧化碳,并防止氨气的溶解,所以用图甲是要“长进长出”,如图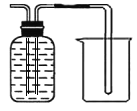 。
。


科目:初中化学 来源: 题型:
【题目】一水泥厂为测定某批石灰石中含碳酸钙的质量分数,称取了12.5g石灰石样品并敲碎,进行了四次高温煅烧(假设其中的固体杂质既没有变化,也没损失).剩余固体质量的数据记录如表:
煅烧次数 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量 | 11.1g | 8.7g | 8.1g | 8.1g |
(注:石灰石煅烧的化学方程式为CaCO3![]() CaO+CO2↑)
CaO+CO2↑)
试计算:
(1)煅烧第______次时,石灰石已完全分解.
(2)石灰石样品中碳酸钙的质量分数____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让NaCl、NH3、CO2 和H2O 尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液)。主要生产流程如下:

(1)“煅烧炉”中发生反应的化学方程式是_______________________。
(2)若在化学实验室里分离“设备(I)”中的混合物,用到的操作名称是____________。
(3)在“设备(Ⅱ)”中固体A与水反应的化学方程式是___________________。
(4)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有______________。(填写化学式)。
(5)请写出一个该生产流程的优点: _________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下图是甲烷燃烧的微观图。

在点燃的条件下,A到B的过程表示的是甲烷分子分解成碳原子和氢原子,氧分子分解成氧原子,B到C的过程表示的是_____________________;
(2)将铝丝浸入CuSO4溶液中,静置,最终观察到的现象是_____________;
(3)在硝酸钡溶液中滴加硫酸溶液,观察反应的现象。反应前后溶液中减少的离子是__________(写离子符号);根据你的分析,在硝酸钡溶液中滴加__________溶液,也会出现相同的实验现象。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学用语书写正确的是
A. 三个二氧化硫分子:2SO3 B. 两个氮分子:2N
C. HClO中氯元素的化合价:![]() D. 一个铝离子:Al+3
D. 一个铝离子:Al+3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】事物之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。
(1)结构决定性质。研究发现含有“过氧基(—O—O—)”的物质具有很强的氧化性,可以作杀菌消毒剂。据此推测,下列物质中,可用作杀菌消毒剂的是 (填数字序号)。
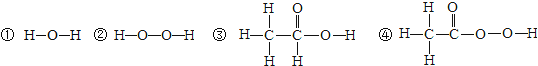
(2)核电荷数为1~18的元素的原子结构示意图等信息如下,回答下列问题:
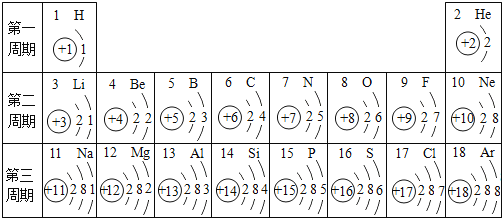
在第3周期中,各原子核外电子排布的变化规律是 。
(3)能将下列物质:“空气、氧气、水蒸气、二氧化碳、高锰酸钾、铁粉、氮气、氧化铁”中的“氧气、铁粉、氮气”分为一类的依据是 。
(4)X元素1个原子的质量是m克,Y元素的相对原子质量为A;化合物XY2的相对分子质量是M,则w克XY2中含有Y的原子数是 。
(5)A、B、C、D、E、F均为初中化学常见的物质,且均含一种地壳中含量最多的元素,其中A是单质;B、C在常温下均为液体,且组成元素相同;E在常温下为气体,有分子构成,能使澄清石灰水变浑浊;反应①中出现火星四射现象。它们之间存在如图所示的转化关系(图中转化条件已略去)。
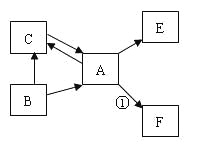
回答有关问题:
①写出B的化学式,并表述显负价元素的化合价: ;
②写出一个属于化合反应的文字表达式或化学方程式 ;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是初中化学常见的实验或操作,回答下列问题:
A. 量筒读数 B.
量筒读数 B. 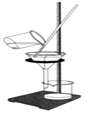 过滤
过滤
C.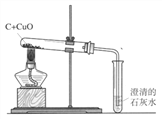 木炭还原氧化铜
木炭还原氧化铜
D.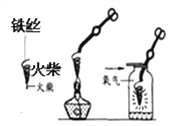 铁丝在氧气中燃烧
铁丝在氧气中燃烧
(1)A实验中读出液体的体积是________mL。
(2)B实验中玻璃棒的作用是__________________。
(3)C实验中看到的实验现象:____________。
(4)D实验把细铁丝盘成螺旋状目的是___________________,集气瓶中放点水的目的是__________ ,铁丝燃烧的化学方程式是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一包白色固体可能含有 Ba(NO3)2、NaCl、NaOH、Na2SO4、CuSO4 中的一种或几种。为确定其组成,某同学设计了如下实验方案:
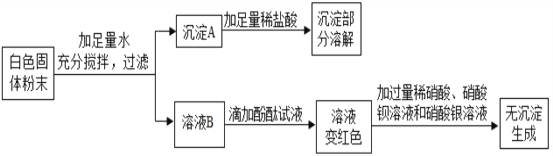
下列判断正确的是
A. 原固体中一定有Ba(NO3)2、NaOH、CuSO4 和Na2SO4
B. 沉淀 A 中一定有Cu(OH)2 和BaSO4
C. 溶液 B 中一定有NaOH 和 Na2SO4,一定没有CuSO4
D. 原固体中一定没有 NaCl和Na2SO4
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是巨大的资源宝库,全球海水中含有的盐类总质量为5亿亿吨,其中含有的各种离子占盐类总质量的百分含量如下表所示:
![]()
某工厂对海水进行综合利用的主要流程如下(本流程涉及的反应均属于复分解反应):

(1)蒸发时为防止液滴飞溅,除了用玻璃棒进行搅拌外,还可以采取的操作是________。
(2)卤水中加入石灰乳发生的主要反应的化学方程式为__________。
(3)己知,试剂A与沉淀B发生的是中和反应,则试剂A的名称为____________; 将卤水转化为溶液C的目的是______________。
(4)某兴趣小组设计了如下实验步骤测定氯化镁的纯度。
①称取9.5g氯化镁样品,放于烧杯中,加足量的水溶解,形成溶液;
②向上述溶液中加入90g质量分数为10%的氢氧化钠溶液;
③充分反应后,过滤;
④将沉淀用蒸馏水洗涤2~3次,洗涤得到的滤液一起并入滤液中;
⑤向最后所得的滤液中加入几滴无色酚酞试液,溶液变红,再逐滴加入10%稀硫酸(密度为1.07g·mL-1),并________,当观察到溶液恰好_______,停止加入稀硫酸;
⑥计算氯化镁样品的纯度。
则步骤④的目的是_______,为计算出氯化镁样品的纯度,除了上述数据外,还需测量的数据是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com