
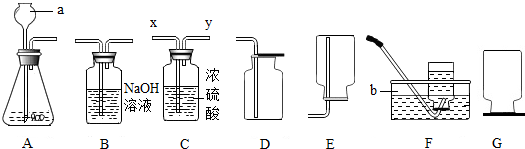


科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
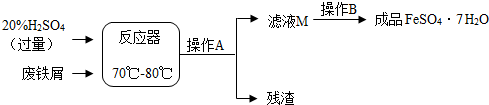
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| 析出 晶体 | FeSO4?7H2O | FeSO4?4H2O | FeSO4?H2O | ||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
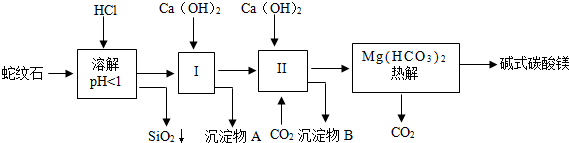
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
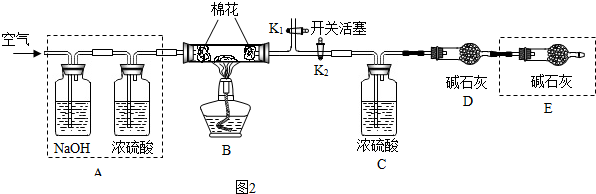
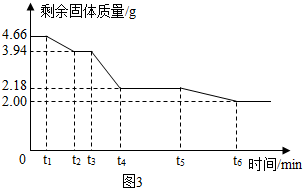
查看答案和解析>>
科目:初中化学 来源: 题型:
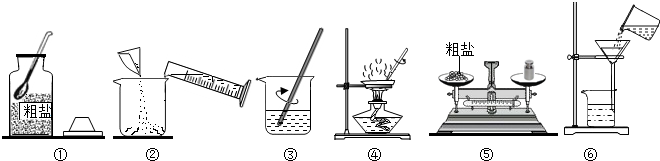
查看答案和解析>>
科目:初中化学 来源: 题型:
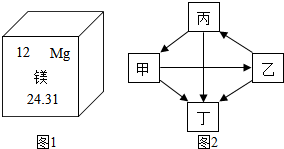
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、洗洁精具有乳化功能,用于去除油污 |
| B、稀硫酸能与金属反应,用于去除铁锈 |
| C、钨的熔点高且能导电,用于制作白炽灯丝 |
| D、一氧化碳有还原性,工业上用来冶炼金属 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com