
| 物质(括号内为杂质) | 操作方法 | |
| A | KCl固体(MnO2) | 加入足量的水溶解,过滤,洗涤,干燥 |
| B | CO气体(CO2) | 通过足量的灼热的氧化铜粉末 |
| C | CaCl2溶液(盐酸) | 加入适量的AgNO3溶液,过滤 |
| D | NaCl溶液(Na2CO3) | 逐滴加入稀盐酸至恰好没有气泡产生 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、KCl固体易溶于水,MnO2难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法错误.
B、CO气体能与灼热的氧化铜粉末反应生成铜和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、CaCl2溶液和盐酸均能与AgNO3溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、Na2CO3能与稀盐酸反应生成氯化钠、水和二氧化碳,至恰好没有气泡产生,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
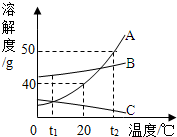 (1)现有A、B、C是那种物质的浓溶液,适用于海水晒盐原理进行结晶的是B
(1)现有A、B、C是那种物质的浓溶液,适用于海水晒盐原理进行结晶的是B查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某气体不能使带火星的木条复燃--该气体一定不含氧气 | |
| B. | 分子可以构成物质--物质一定是由分子构成的 | |
| C. | 混合物由多种物质组成--混合物中一定含有多种元素 | |
| D. | 中和反应有盐和水生成--有盐和水生成的反应不一定是中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 实验目的 | 实验过程 |
| ① | 除去变质杂质 | 取溶液,滴加石灰水至恰好完全反应,过滤 |
| ② | 确定变质后成分 | 取少量溶液,加入石灰水,过滤,向滤液中滴加酚酞溶液 |
| ③ | 证明已经变质 | 取少量溶液,滴加盐酸,将生成的气体通入澄清的石灰水 |
| ④ | 测定变质后的纯度 | 取一定量溶液,加入盐酸,用氢氧化钠固体吸收气体,称量 |
| A. | ②③ | B. | ①③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 鼓励使用太阳能、风能等清洁能源能减少PM2.5的污染 | |
| B. | 明矾可使水中悬浮小颗粒快速沉降,也可用于自来水的消毒杀菌 | |
| C. | 发酵粉中含有较多的NaHCO3,能使焙制出的糕点疏松多孔 | |
| D. | 纯碱也叫苏打,可用于清洗厨房用具的油污 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 煤、石油和天然气等化石燃料是目前人类使用的最主要燃料,也是重要的化工原料.
煤、石油和天然气等化石燃料是目前人类使用的最主要燃料,也是重要的化工原料.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 滴数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| PH | 13.4 | 13.3 | 13.2 | 13.0 | 12.8 | 12.96 | 12.4 | 4.5 | 1.6 | 1.4 | 1.3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com