
| A. | 同温度同质量液态水和玻璃态水,体积相同 | |
| B. | 玻璃态水不属于氧化物 | |
| C. | 玻璃态水和普通水的化学性质相同 | |
| D. | 玻璃态水分子不运动 |
分析 A、根据玻璃态水与液态水密度的关系考虑.
B、根据水的组成结构及氧化物质的定义判断.
C、根据玻璃态水与普通水的成分分析.
D、玻璃态的水中的水分子具有微观粒子的性质,分子是不断运动的.
解答 解:A、由玻璃态的水密度与普通液态水的密度相同,所以同温度同质量液态水和玻璃态水,体积相同,故正确;
B、氧化物是指由两种元素组成,并且其中一种为氧元素的化合物,而玻璃态的水是由氢氧两种元素组成的化合物,所以错误;
C、玻璃态水与普通水的成分一样,所以化学性质相同,所以正确;
D、玻璃态的水中的水分子具有微观粒子的性质,分子是不断运动的,故C错误.
故选AC.
点评 物质的分类是重点的基础化学知识,但却是学习难点之一,要能正确地、合理地对物质作出正确分类,首先要理解物质分类的有关概念,抓住概念间的相互关系和本质区别.


科目:初中化学 来源: 题型:解答题
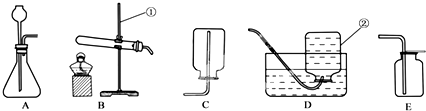
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
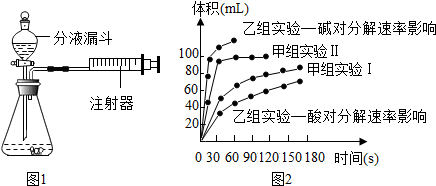
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2% H2O2 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5% H2O2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
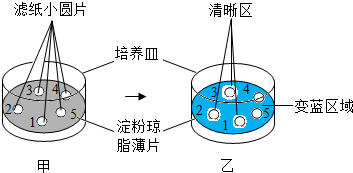 某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:
某科学兴趣小组从浸泡后的绿豆中提取淀粉酶溶液,为了研究酸碱性对该淀粉酶催化作用的影响,以淀粉琼脂为材料进行实验,步骤如下:| 滤纸编号 | 溶液成分 |
| 1 | 淀粉酶溶液 |
| 2 | 淀粉酶溶液-稀盐酸 |
| 3 | 淀粉酶溶液-稀碳酸钠溶液 |
| 4 | 稀盐酸 |
| 5 | 稀碳酸钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
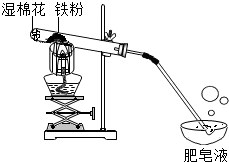 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 实验操作 | 实验现象及结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
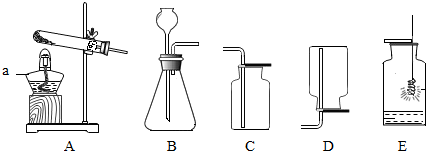
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 试剂、方法 |
| A | MnO2 | 炭粉 | 在空气中灼烧 |
| B | CO2 | CO | 点燃 |
| C | FeSO4 | CuSO4 | 加入足量铁屑,充分反应后过滤 |
| D | CaO | CaCO3 | 高温 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com