
 ijͬѧ��ʵ���ҷ���һƿ��ǩ��ȱ����ͼ1��ʾ������Һ��Ϊ�˲ⶨ����Һ������������������ȡ��10g����Һ����������μ���������������Ϊ20%��NaOH��Һ����Ӧ��������Һ��pH������NaOH��Һ�����Ĺ�ϵ��ͼ2��ʾ��
ijͬѧ��ʵ���ҷ���һƿ��ǩ��ȱ����ͼ1��ʾ������Һ��Ϊ�˲ⶨ����Һ������������������ȡ��10g����Һ����������μ���������������Ϊ20%��NaOH��Һ����Ӧ��������Һ��pH������NaOH��Һ�����Ĺ�ϵ��ͼ2��ʾ������ ��1��A���ⶨ��Һ��������pH��ֽ��B����̪��Һ���ڼ�������Һ��C��ʯ����Һ���ڼ��������Һ��
��2������A����Һp����7�������
��3������ϡH2SO4��NaOH��Һ�ķ�Ӧ�ķ���ʽ����NaOH���������ϡH2SO4����Һ�к�H2SO4�����������������ϡH2SO4����������������
��� �⣺��1��A���ⶨ��Һ��������pH��ֽ��B����̪��Һ���ڼ�������Һ��C��ʯ����Һ���ڼ��������Һ��
���A��
��2����ͼʾ��֪����a��ʱ��Һ��pH����7��˵�������NaOH������������ȫ��Ӧ��û��ʣ�࣬������Һ�к��е������У�Na2SO4��NaOH��
���Na2SO4��NaOH��
��3����ͼʾ��֪������Һ��pH����7�����ĵ�NaOH��Һ������Ϊ8g�����ʵ�����Ϊ��8g��20%=1.6g��10gϡ������Ʒ����H2SO4������Ϊx
2NaOH+H2SO4�TNa2SO4+2H2O
80 98
1.6g x
$\frac{80}{1.6g}$=$\frac{98}{x}$
��ã�x=1.96g
ϡH2SO4��������������Ϊ��$\frac{1.96g}{10g}$��100%=19.6%
��ϡH2SO4����������������19.6%��
���� ������һ�����ͼ��ļ����⣬����ʱ�ҵ�pH=7��ǡ�÷�Ӧ�㣬�����û�ѧ����ʽ�ļ�����н���ǽ����ͻ�ƿڣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
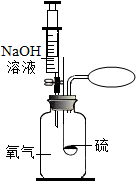 ijͬѧ����������������ȼ�ա���ʵ��ʱ��Ϊ�˷�ֹ������Ⱦ��������������Һ �����ն������������Ǹ�ͬѧʵ���������̣�
ijͬѧ����������������ȼ�ա���ʵ��ʱ��Ϊ�˷�ֹ������Ⱦ��������������Һ �����ն������������Ǹ�ͬѧʵ���������̣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ƻ�� | B�� | ֲ���� | C�� | ��ˮ | D�� | ʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 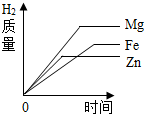 ��������Mg��Zn��Fe��������ϡ���ᷴӦ | |
| B�� | 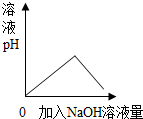 NaOH��Һ��μ���ϡ������ | |
| C�� | 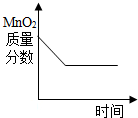 ��������غͶ������̵Ļ���� | |
| D�� | 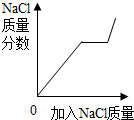 ������ӽ����͵�NaCl��Һ�м���NaCl���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ù���к�ǿ�Ķ��� | |
| B�� | ����ù����̼���⡢��Ԫ�ص�������Ϊ17��12��6 | |
| C�� | ����ù�����л��� | |
| D�� | 1������ù�ط�����35��ԭ�ӹ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com