
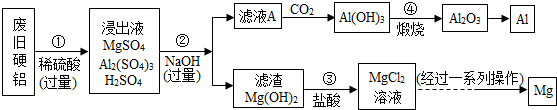
·ÖĪö £Ø1£©øł¾ŻĆ¾ŗĶĮņĖį·“Ó¦»įÉś³ÉĮņĖįĆ¾ŗĶĒāĘų£¬ĀĮŗĶĮņĖį·“Ӧɜ³ÉĮņĖįĀĮŗĶĒāĘų½ųŠŠ·ÖĪö£»
£Ø2£©øł¾Ż¹żĀĖæÉŅŌ½«¹ĢĢåŗĶŅŗĢå½ųŠŠ·ÖĄė£¬ŅŌ¼°¹żĀĖŠčŅŖµÄŅĒĘ÷½ųŠŠ·ÖĪö£»
£Ø3£©øł¾ŻĒāŃõ»ÆĆ¾ŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆĆ¾ŗĶĖ®½ųŠŠ·ÖĪö£»
£Ø4£©øł¾ŻĒāŃõ»ÆĀĮģŃÉÕÉś³ÉĮĖŃõ»ÆĀĮŗĶĖ®½ųŠŠ·ÖĪö£»
£Ø5£©øł¾ŻĀĮŗĶ»ÆѧŠŌÖŹ·Ē³£»īĘĆ½ųŠŠ·ÖĪö£®
½ā“š ½ā£ŗ£Ø1£©Ć¾ŗĶĮņĖį·“Ó¦»įÉś³ÉĮņĖįĆ¾ŗĶĒāĘų£¬ĀĮŗĶĮņĖį·“Ӧɜ³ÉĮņĖįĀĮŗĶĒāĘų£¬¹żĮæµÄĻ”ĮņĖįæÉŅŌČܽāĆ¾ŗĶĀĮ£¬»Æѧ·½³ĢŹ½ĪŖ£ŗMg+H2SO4=MgSO4+H2”ü”¢2Al+3H2SO4=Al2£ØSO4£©3+3H2”ü£»
£Ø2£©¹żĀĖæÉŅŌ½«¹ĢĢåŗĶŅŗĢå½ųŠŠ·ÖĄė£¬¾¹ż²½Öč¢ŚŗóµĆµ½ĮĖ¹ĢĢåŗĶŅŗĢ壬ĖłŅŌ·ÖĄė²Ł×÷ĪŖ¹żĀĖ£¬¹żĀĖŠčŅŖµÄŅĒĘ÷ÓŠÉÕ±”¢Ā©¶·”¢²£Į§°ō£»
£Ø3£©ĒāŃõ»ÆĆ¾ŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆĆ¾ŗĶĖ®£¬»Æѧ·½³ĢŹ½ĪŖ£ŗMg£ØOH£©2+2HCl=MgCl2+2H2O£»
£Ø4£©ĒāŃõ»ÆĀĮģŃÉÕÉś³ÉĮĖŃõ»ÆĀĮŗĶĖ®£¬Āś×ć·Ö½ā·“Ó¦Ņ»±ä¶ąµÄĢõ¼ž£¬ŹōÓŚ·Ö½ā·“Ó¦£»
£Ø5£©ĀĮ¾ßÓŠŗÜŗĆæ¹øÆŹ“ŠŌµÄŌŅņŹĒ£ŗĀĮŗĶæÕĘųÖŠµÄŃõĘų·“Ӧɜ³ÉÖĀĆܵÄŃõ»ÆĀĮ±”Ĥ£®
¹Ź“š°øĪŖ£ŗ£Ø1£©Mg+H2SO4=MgSO4+H2”ü”¢2Al+3H2SO4=Al2£ØSO4£©3+3H2”ü£»
£Ø2£©¹żĀĖ£¬Ā©¶·£»
£Ø3£©Mg£ØOH£©2+2HCl=MgCl2+2H2O£»
£Ø4£©·Ö½ā·“Ó¦£»
£Ø5£©ĀĮŗĶæÕĘųÖŠµÄŃõĘų·“Ӧɜ³ÉÖĀĆܵÄŃõ»ÆĀĮ±”Ĥ£®
µćĘĄ ±¾Ģāæ¼²éĮĖÓŠ¹Ų½šŹōµÄŠŌÖŹ£¬ŹģĮ·ÕĘĪÕ½šŹō»ī¶ÆŠŌĖ³ŠņµÄŅāŅ壬ĮķĶāŌŚ½ā“ĖĄąĢāŹ±£¬Ź×ĻČ·ÖĪöĢāÖŠæ¼²éµÄĪŹĢā£¬Č»ŗó½įŗĻѧ¹żµÄÖŖŹ¶ŗĶĢāÖŠĖłøųµÄ׏ĮĻ½ųŠŠ½ā“š£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »šµÄ·¢ĻÖŗĶĄūÓĆ | B£® | ÖʵĆĮĖĶĘ÷ | C£® | ¾ĘµÄÄšÖĘ | D£® | ŗŚ»šŅ©µÄ·¢Ć÷ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
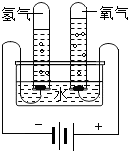 ČēĶ¼ŹĒĖ®Ķصē·Ö½āµÄ×°ÖĆŹ¾ŅāĶ¼£ŗ
ČēĶ¼ŹĒĖ®Ķصē·Ö½āµÄ×°ÖĆŹ¾ŅāĶ¼£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ų·æÖŠÓĆŹ³“×¼ų±š“æ¼īŗĶŹ³ŃĪ | |
| B£® | ÓĆAgNO3ČÜŅŗ¼ų±šH2ÖŠ»ģČėµÄÉŁĮæHClŌÓÖŹ | |
| C£® | ÓĆĻ”ĮņĖį³żČ„Ģś·ŪÖŠ»ģÓŠµÄÉŁĮæĶ·Ū | |
| D£® | ÓĆĻ”ŃĪĖį¼ģŃ鱩Ā¶ŌŚæÕĘųÖŠµÄNaOH¹ĢĢåŹĒ·ń±äÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
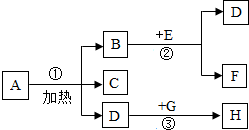 ŌŚČēĶ¼×Ŗ»Æ¹ŲĻµÖŠ£¬Éś³ÉĪļDÄÜŹ¹“ų»šŠĒµÄľĢõø“Č¼£¬HÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ŌŚ·“Ó¦?ÖŠ£¬BµÄÖŹĮæŗĶ»ÆѧŠŌÖŹ¾łĆ»ÓŠøı䣮
ŌŚČēĶ¼×Ŗ»Æ¹ŲĻµÖŠ£¬Éś³ÉĪļDÄÜŹ¹“ų»šŠĒµÄľĢõø“Č¼£¬HÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£¬ŌŚ·“Ó¦?ÖŠ£¬BµÄÖŹĮæŗĶ»ÆѧŠŌÖŹ¾łĆ»ÓŠøı䣮²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com