
| A. | 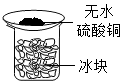 装置验证空气中有水分 | B. | 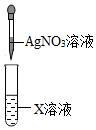 装置验证X溶液中是否含有Cl- | ||
| C. | 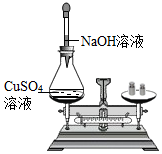 装置验证质量守恒定律 | D. | 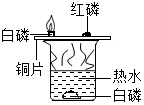 装置验证可燃物燃烧的两个条件 |
分析 A、根据无水硫酸铜遇水变蓝,进行分析判断.
B、根据检验溶液中是否含有Cl-,可用酸化的硝酸银溶液,进行分析判断.
C、根据氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,进行分析判断.
D、根据薄铜片上的白磷和红磷、水中的白磷的燃烧情况,进行分析判断.
解答 解:A、烧杯中的冰块起着降温的作用,能冷凝空气中的水蒸气,无水硫酸铜遇到水蒸气变蓝,甲装置可以验证空气中有水分,故选项实验能达到实验目的.
B、检验某溶液中是否含有Cl-,可用酸化的硝酸银溶液,一般用硝酸银溶液和稀硝酸,若产生白色沉淀,说明含有氯离子,故选项实验不能达到实验目的.
C、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,能用于验证质量守恒定律,故选项实验能达到实验目的.
D、铜片的白磷燃烧,红磷不燃烧,水中的白磷不能燃烧,薄铜片上的白磷能与氧气接触,温度能达到着火点,水中的白磷不能与氧气接触,红磷温度没有达到着火点;可得出燃烧需要与氧气接触,且温度达到着火点,故选项实验能达到实验目的.
故选:B.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 4.0 | m | 0.6 | 0.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com