
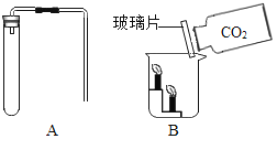
【题目】化学兴趣小组的同学设计并进行了CO2的制取与性质的实验。如图A,检查装置的气密性,操作为_____,观察到导管口有气泡冒出。然后加入药品,固定装置,制取CO2,有关化学方程式_____。如图B,现象为_____,说明CO2的性质是_____。由此推知,一般情况下可燃物燃烧的条件之一是_____。
【答案】将导管末端浸入水中,用手或热毛巾捂热试管,观察导管口是否气泡冒出 CaCO3+2HCl=CaCl2+H2O+CO2↑ 蜡烛由低到高渐次熄灭 密度比空气大、不能燃烧也不支持燃烧 与氧气接触
【解析】
凡是制取气体的装置都要检查装置的气密性,如图A,检查装置的气密性的操作为:将导管末端浸入水中,用手或热毛巾捂热试管,观察到导管口是否有气泡冒出。然后加入药品,固定装置,制取CO2,实验室常用大理石和稀盐酸反应制取二氧化碳,有关化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑.如图B由现象为:蜡烛由低到高渐次熄灭,说明CO2的性质是密度比空气大、不能燃烧也不支持燃烧。由于此实验中二氧化碳将蜡烛与氧气隔开,蜡烛的熄灭可推知,一般情况下可燃物燃烧的条件之一是与氧气接触。
故答为:将导管末端浸入水中,用手或热毛巾捂热试管;CaCO3+2HCl=CaCl2+H2O+CO2↑;蜡烛由低到高渐次熄灭;密度比空气大、不能燃烧也不支持燃烧;与氧气接触。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
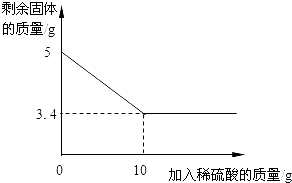
【题目】某同学称量5g木炭粉与氧化铜高温加热一段时间后的剩余固体于烧杯中,向烧杯中加入稀硫酸,发现烧杯中剩余固体的质量与加入稀硫酸质量的关系如图所示:
回答下列问题:
(1)木炭粉与氧化铜反应一段时间后剩余固体中除Cu外,一定含有的物质是 ,该物质在剩余固体中的质量分数是 。
(2)求所加稀硫酸的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出蜡烛在氧气中燃烧的化学反应文字表达式: 。
(2)探究一:蜡烛燃烧产生火焰的原因是什么?

点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图所示)。由此可知:蜡烛燃烧产生的火焰是由 (填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
【查阅资料】
由该表可知:物质燃烧能否产生火焰与其 (填“熔点”或“沸点”)和燃烧时温度有关。由此推测:钠在燃烧时, (填“有”或“没有”)火焰产生。
(4)木炭在氧气中燃烧没有火焰,但生活中同样的木炭燃烧时会产生火焰,其原因可能是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有科学家研究发现,氧气可通过高能真空紫外线照射二氧化碳直接产生,该化学反应模型如图所示,关于该反应的说法正确的是( )
![]()
A. 反应物和生成物都由分子构成B. 该反应的最小微粒是分子
C. 该反应属于化合反应D. 为制取氧气提供了新方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小乐利用图示实验装置测定某大理石样品的纯度(所含杂质不与盐酸反应,且不溶于水)。她取了该大理石样品12.5g,并加入足量稀盐酸进行实验。实验数据记录如下表:
时间/s | 0 | 20 | 30 | 40 |
装置和药品的总质量/g | 117.9 | 114 | 113.5 | 113.5 |

(1)反应共生成CO2的质量为______g。
(2)计算该大理石样品中CaCO3的质量分数______。(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
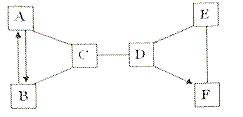
【题目】A~F是初中化学常见的物质,已知A、B、C、D、E是五种不同类别的物质,A是空气中含有的一种气体,E是地壳中含量最多的金属元素组成的单质,F中各元素质量比为2:1:2,六种物质之间的反应与转化关系均为初中化学常见的化学反应,图中“﹣”表示相连的物质能相互反应,“→”表示一种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)请回答下列问题:
(1)E物质的化学式_____。
(2)A和C反应的化学方程式_____。
(3)E和F反应的化学方程式_____。
(4)如图所有的化学反应中涉及到的基本反应类型有_____种。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌。右下图横坐标x表示N物质的质量,纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对应关系合理的是
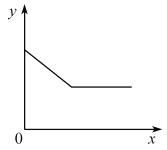
M | N | y | |
A | 水 | 氧化钙 | 溶液的温度 |
B | 水 | 氢氧化钠 | 溶液的pH |
C | 饱和氯化钠溶液 | 氯化钠 | 溶液的溶质质量分数 |
D | 硫酸铜溶液 | 铁粉 | 溶液的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语填空。
(1)2个氢原子_____________(2)氖气_____________
(3)4个亚铁离子_____________(4)N2O5中氮元素的化合价_____________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】侯德榜是我国著名的化学家。由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质。某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案
方案一:称取样品10.65g,加水完全溶解,向其中加入足量的氯化钡溶液,发生如下反应Na2CO3+BaCl2=BaCO3↓+2NaCl
充分反应后,过滤、洗涤,干燥得固体19.70g.通过计算(写出计算过程)判断该厂的产品是否属于优等品。(杂质可溶于水且不与氯化钡反应)
方案二:用如图所示的装置,通过准确测量排出水的体积,也可计算样品的纯度。称取纯碱固体2.0g,加入足量的稀硫酸,发生如下反应:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑,完全反应,使气体放出,测得量筒中水的体积为330毫升,请你计算样品的纯度(本题中二氧化碳的密度取2.0g/L)
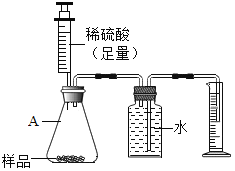
(1)请任意选择一种方案进行计算。________
(2)同学分析发现方案二所测的碳酸钠纯度偏低,造成此结果的原因可能是______(装置的气密性良好)
A A装置中残留反应产生的二氧化碳气体 B 部分CO2溶于水或与水反应
C 与量筒相连的导管中有水 D 量筒读数时,俯视读数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com