
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 在装有过氧化氢溶液的试管口,放一个带火星的木条 | 木条不复燃 | 常温下过氧化氢溶液分解速率慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 水泥块能作过氧化氢分解的催化剂 |
分析 根据过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
根据催化剂是在化学变化中能改变其它物质的化学反应速率,而本身的质量和化学性质在反应前后都没有改变的物质,要验证是否是催化剂,除了能加快反应速率外,质量和化学性质也不能发生改变等知识进行分析.
解答 解:过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
【实验验证】
| 实验一 | 在装有过氧化氢溶液的试管口,放一个带火星的木条 | 木条不复燃 | 常温下过氧化氢溶液分解速率慢 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 水泥块能作过氧化氢分解的催化剂 |
| 实验一 | 在装有过氧化氢溶液的试管口,放一个带火星的木条 | ||
| 实验二 | 水泥块能作过氧化氢分解的催化剂 |
点评 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.


科目:初中化学 来源: 题型:选择题
| A. | 铁矿石在地壳中含量丰富,可以随意开采 | |
| B. | 废弃铁制品再利用的成本太高,属于不可回收垃圾 | |
| C. | 为防止铁制品生锈,可在其表面涂上一层油漆 | |
| D. | 钢的含碳量比生铁的高,所以钢的性能比生铁优越 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
学习化学一年后,同学们对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”以及“支持燃烧的气体一般是氧气”这两句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
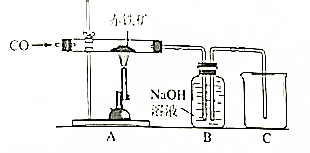 某化学小组利用CO模拟冶炼铁的原理(如图所示)
某化学小组利用CO模拟冶炼铁的原理(如图所示)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
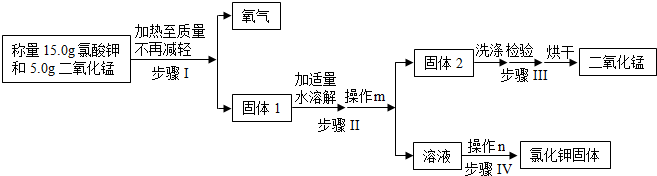
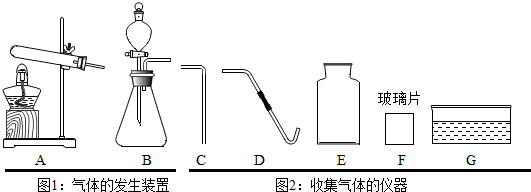
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
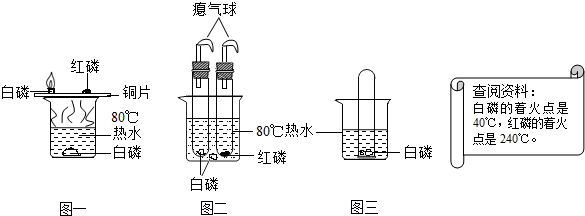
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 拉瓦锡测定空气中氧气的含量 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O5 化合反应 | |
| B. | 比较铜和银的金属活动性 Cu+2AgNO3═Cu(NO3)2+2Ag 置换反应 | |
| C. | 用硫酸除铁锈 Fe2O3+2H2SO4═2FeSO4+3H2O 置换反应 | |
| D. | 煅烧石灰石制生石灰 CaCO3═CaO+CO2↑ 分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com