
| 实验步骤 | 实验现象 | 实验结论 |
| 实验一:取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸) | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl,(Na2CO3+2HCl═2NaCl+H2O+CO2↑) |
| 实验二:取少量溶液于试管中,滴加硫酸铜溶液 | 产生蓝色沉淀 | 该溶液是氢氧化钠溶液. |
分析 (1)氢氧化钙常温下的溶解度为0.18g,据此可计算出其饱和溶液的质量分数达不到10%,所以可判断不可能为氢氧化钙;
(2)从题目中分析,氢氧化钠、氯化钠、碳酸钠中只有氯化钠是盐,其余两种都是碱,所以应该是加入酸碱指示剂判断是否为氯化钠;
(3)鉴别氢氧化钠和碳酸钠,可以用氯化钙溶液,能产生碳酸钙沉淀,也可以采用稀盐酸,能产生气体,两种方法都可以;
从题中可得到很多反思,如实验需要有严谨的态度.
解答 解:(1)常温下氢氧化钙的溶解度为0.18g,其饱和溶液中溶质质量分数=$\frac{0.18g}{100g+0.18g}$×100%<0.18%,而该溶液溶质质量分数为10%,所以不可能是氢氧化钙;
(2)从题中分析,能使试液变红色,指示剂为无色酚酞,而氯化钠是盐,显中性,不能使无色酚酞试液变红色,可以排除氯化钠;
(3)氯化钙和稀盐酸都可以用来鉴别氢氧化钠和碳酸钠,氯化钙与碳酸钠反应产生碳酸钙白色沉淀,方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl,稀盐酸与碳酸钠反应产生二氧化碳气体,方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【实验反思】实验二的设计不合理.因为碳酸钠与氢氧化铜反应也能生成蓝色沉淀.
故答案为:(1)Ca(OH)2微溶于水,常温下不可能得到10%的氢氧化钙溶液;
(2)无色酚酞;NaCl;NaCl溶液呈中性,不能使无色酚酞试液变红色;
(3)实验步骤:氯化钙溶液(或稀盐酸)
实验现象:产生白色沉淀(或有气泡冒出)
实验结论:CaCl2+Na2CO3═CaCO3↓+2NaCl,(Na2CO3+2HCl═2NaCl+H2O+CO2↑);
【实验反思】不合理.因为碳酸钠与氢氧化铜反应也能生成蓝色沉淀.
.
点评 本题是缺失标签的实验探究题,根据氢氧化钠、氯化钠、氢氧化钙、碳酸钠几种物质的性质特点,采取“利用测定结果进行先排除,最后进行实验检验的”方法确定未知溶液,涉及对四种物质相关性质及变化规律的考查.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
| 残留固体的成分 | 探究的步骤 | 可能观察到的现象 | 结论及化学反应方程式 |
| (1)可能有氧化钙. | 取残留固体加水溶解,过滤,向滤液中滴加几滴无色酚酞试液. | 现象: | 结论: |
| (2)还可能有碳酸钙. | 另取残留固体滴加足量盐酸. | ① | 结论: 方程式: |
| ② | 结论: |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
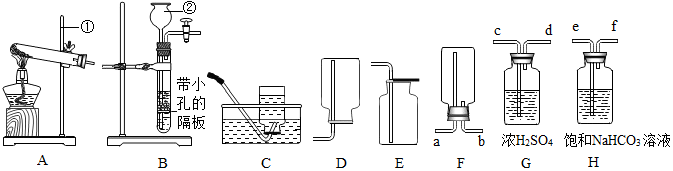
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
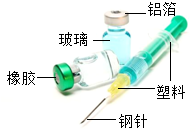 如图所示是医院常用的药瓶和注射器,请你据图回答:
如图所示是医院常用的药瓶和注射器,请你据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 名称 | 俗名 | 化学式 |
| A | 氢氧化钠 | 烧碱 | NaOH |
| B | 碳酸氢钠 | 苏打 | NaHCO3 |
| C | 氢氧化钙 | 熟石灰 | CaO |
| D | 乙醇 | 酒精 | CH3COOH |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com