【答案】
分析:(1)用盐酸除铁锈:先弄清铁锈的主要成分氧化铁,则可知反应物为氧化铁与盐酸,反应符合复分解反应的特点,则可知生成物为氯化铁和水;
(2)红磷燃烧:知反应物为磷和氧气,反应条件为点燃,生成物为五氧化二磷;
(3)铁棒插入氯化铜溶液中:则知反应物为铁与氯化铜,生成物为氯化亚铁和铜;
(4)加热高锰酸钾固体:则可知反应物为高锰酸钾,生成物为锰酸钾、二氧化锰、氧气,反应条件为加热;
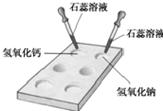
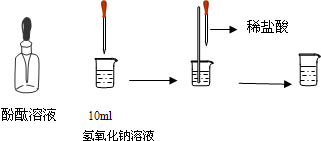
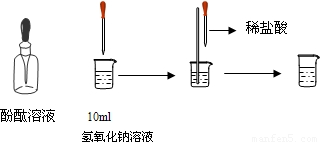
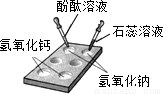
(5)利用天津碱厂的碱渣(含有熟石灰)制取少量烧碱:根据复分解反应的特点,结合质量守恒定律,可知反应物为碳酸钠与氢氧化钙,生成物为氢氧化钠与碳酸钙.
解答:解:(1)用盐酸除铁锈:由题意可知,反应物,反应符合复分解反应的特点,则可知生成物,故此反应的化学方程式为Fe
2O
3+6HCl=2FeCl
3+3H
2O;
(2)红磷燃烧:知反应物,反应条件,生成物,故此反应的化学方程式为4P+5O
2
2P
2O
5;
(3)铁棒插入氯化铜溶液中:知反应物,生成物,故此反应的化学方程式为Fe+CuCl
2=FeCl
2+Cu;
(4)加热高锰酸钾固体:知反应物,反应条件,生成物,故此反应的化学方程式为2KMnO
4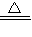
K
2MnO
4+MnO
2+O
2↑;
(5)熟石灰制取少量烧碱:知反应物,生成物,故此反应的化学方程式为Na
2CO
3+Ca(OH)
2=2NaOH+CaCO
3↓
故答为:(1)Fe
2O
3+6HCl=2FeCl
3+3H
2O;
(2)4P+5O
2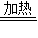
2P
2O
5;
(3)Fe+CuCl
2=FeCl
2+Cu
(4)2KMnO
4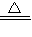
K
2MnO
4+MnO
2+O
2↑;
(5)Na
2CO
3+Ca(OH)
2=2NaOH+CaCO
3↓
点评:确定反应物、生成物、反应条件,正确书写化学方程式;并且掌握书写化学方程式的方法和步骤;学会从题目中提取有效的信息.

 2P2O5;
2P2O5;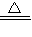 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;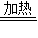 2P2O5;
2P2O5;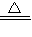 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;