
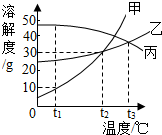
 甲乙丙三种固体物质的溶解度曲线如图所示,回答下列问题.
甲乙丙三种固体物质的溶解度曲线如图所示,回答下列问题.分析 (1)据该温度下甲的溶解度分析解答;
(2)丙溶解度随温度升高而减小,所以使其不饱和溶液变为饱和溶液的方法有增加溶质、蒸发溶剂、升温;
(3)据饱和溶液中溶质的分数的计算式$\frac{溶解度}{溶解度+100g}$×100%可知:饱和溶液中溶解度相等则溶质的质量分数相等;
(4)据二者的溶解度随温度变化及饱和溶液中溶质的 质量分数计算方法解答.
解答 解:(1)t1℃时甲的溶解度是10g,即100g水中溶解10g的甲恰好饱和,所以甲物质的饱和溶液中溶质与溶剂的质量比为10g:100g=1:10;
(2)丙溶解度随温度升高而减小,所以使其不饱和溶液变为饱和溶液的方法有增加溶质、蒸发溶剂、升温;
(3)据饱和溶液中溶质的分数的计算式$\frac{溶解度}{溶解度+100g}$×100%可知:饱和溶液中溶解度相等则溶质的质量分数相等;所以要配置相同溶质质量分数的甲和乙的饱和溶液,二者温度须相等,则温度控制在 t2℃,此时二者的溶解度相等;
(4)t2℃时乙、丙的饱和溶液同时升温至t3℃,乙的溶解度变大,溶质、溶剂的质量不变,溶质质量分数与升温前相等,丙溶解度减小,析出溶质,由(2)可知饱和溶液中溶解度大则溶质的质量分数大,t3℃时丙的溶解度大于t2℃乙的溶解度,则所得溶液中溶质的质量分数大小关系为:乙<丙;
故答案为:(1)1:10; (2)加入丙(或蒸发溶剂、升温); (3)t2; (4)<.
点评 明确溶解度概念、饱和溶液中溶解度大则溶质质量分数大,不饱和溶液与饱和溶液之间的相互转化等知识,并能灵活运用解答相关问题.


科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作步骤 | 预期实验现象 | 预期结论 |
| 另取适量样品溶液于试管中,滴加氯化钡溶液(或氯化钙溶液)至不再产生沉淀为止,静置;取上层清液,加入酚酞溶液. | 产生白色沉淀;溶液变红(或溶液不变色) | 氢氧化钠部分变质(或氢氧化钠全部变质) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入 稀盐酸 | 有气泡产生 | 滤液中含有K2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图甲装置,请回答下列问题:
如图甲装置,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com