
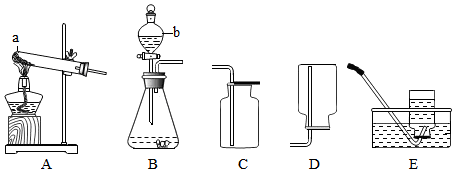
| 实验序号 | ① | ② | ③ | ④ |
| ag大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| bg盐酸 | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
(3)根据制取气体时,组装好仪器后,应先检验装置气密性,再添加药品;选择气体的收集方法时,需要考虑的因素是气体的密度和溶解性进行分析;
(4)根据实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳的密度比空气大,溶于水,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
根据控制变量法的具体操作进行分析;
(5)根据实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,极易溶于水进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是试管,b是分液漏斗;
(2)实验室用过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,所以选择的发生装置是B,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)制取气体时,组装好仪器后,应先检验装置气密性,再添加药品;选择气体的收集方法时,需要考虑的因素是气体的密度和溶解性;
(4)实验室制取二氧化碳的反应物是固体和液体,反应条件是常温,二氧化碳的密度比空气大,溶于水,所以发生装置选B,收集装置选C,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
实验①与③对照,可以探究固体反应物颗粒大小对反应速率的影响,上述实验中,另一个影响反应速率的因素是:盐酸的浓度;
(5)实验室制取氨气的反应物是固体,反应条件是加热,氨气密度比空气小,极易溶于水,所以制取一瓶氨气所需要选用的装置组合是AD.
故答案为:(1)试管,分液漏斗;
(2)B,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)检验装置气密性,气体的密度,溶解性;
(4)反应物是固体和液体,反应条件是常温,C,CaCO3+2HCl=CaCl2+H2O+CO2↑;
③,盐酸的浓度;
(5)AD.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:选择题
| A. | 假设 | B. | 实验 | C. | 观察 | D. | 作出结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 小明用如图电解水的简易装置来研究水的组成.请回答下列问题:
小明用如图电解水的简易装置来研究水的组成.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
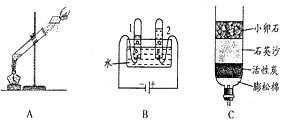 水是人类最宝贵的自然资源.没有水就没有生命,根据你所掌握的有关水的知识回答下列问题:
水是人类最宝贵的自然资源.没有水就没有生命,根据你所掌握的有关水的知识回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是由氢气分子和氧气分子组成 | B. | 电解水是将化学能转化为电能 | ||
| C. | 煮沸可以使大多数硬水软化 | D. | 明矾可用于吸附水中的色素和异味 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com