
下列说法正确的是( )
①所有原子的原子核都是由质子和中子构成的 ②在同一种物质中同种元素的化合价可能不相同 ③由同一种元素组成的物质一定是单质,不可能是化合物 ④分子、原子都是不带电的粒子,所以不带电的粒子一定是分子或原子 ⑤NH3中氮元素的化合价为-3 ⑥粒子结构示意图 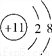 表示的是一种金属阳离子
表示的是一种金属阳离子
A. ①②③ B. ④⑤⑥ C. ②⑤⑥ D. ①③④
C 【解析】①不是所有原子的原子核都是由质子和中子构成,例如氢原子不含有中子,错误;②在同一种物质中同种元素的化合价可能不相同,例如硝酸铵中,氮元素的化合价有-3和+5价,正确;③由同一种元素组成的物质不一定是单质,有可能是混合物,错误;④不带电的粒子不一定是分子或原子,还可能是中子,错误;⑤根据化合物中元素正负化合价的代数和为零,NH3中氢为+1价,氮元素为-3价,正确;⑥由粒子的结构示意...科目:初中化学 来源:陕西省西安市碑林区2014-2015学年九年级第二次模拟考试化学 题型:填空题
人类的生产生活离不开金属材料。
(1)铜和铁一样也可以生锈,铜锈的主要成分是碱式碳酸铜[Cu2(OH)2CO3],是铜与空气中的氧气、水和________(填化学式)共同作用的结果。
(2)向铜锈中加入过量稀硫酸,固体逐渐溶解,得到蓝色硫酸铜溶液,从蓝色溶液中回收铜的过程如下:
 第
第
①向蓝色溶液中加入过量铁粉,发生反应的化学方程式是_________________________;
②操作a是________。
CO2 Fe+CuSO4=== FeSO4+Cu 过滤 【解析】(1)由于铜锈的组成元素含有氢、碳元素,结合空气的成分可知:碱式碳酸铜[化学式为Cu2(OH)2CO3,是铜与空气中氧气、H2O 及CO2 共同作用的结果;(2)①硫酸铜与铁反应生成了硫酸盐亚铁和铜,反应的方程式是:Fe+CuSO4=FeSO4+Cu;②在蓝色溶液中回收铜的过程中,通过操作a从固液混合物中得到了固体,所以,操作a...查看答案和解析>>
科目:初中化学 来源:江苏省苏州市2017~2018学年初三化学第二次模拟测试卷(1) 题型:单选题
洗发产品中含有的枸橼酸(C6H8O7)能使头发柔顺有弹性且气味清香。下列关于枸橼酸的说法正确的是
A. 枸橼酸由 6 个碳原子、8 个氢原子和 7 个氧原子构成
B. 枸橼酸属于有机高分子化合物
C. 枸橼酸中氧元素的质量分数最大
D. 枸橼酸中碳、氢、氧三种元素的质量比为 6:8:7
C 【解析】A、枸橼酸是由枸橼酸分子构成的,而不是由原子直接构成的,错误; B、有机高分子化合物是相对分子质量能达几万至几十万的化合物,所以枸橼酸不属于有机高分子化合物,错误; C、枸橼酸C6H8O7中C、H、O三种元素的质量比=(12×6):(1×8):(16×7)=9:1:14,可见氧元素的质量分数最大,正确; D、枸橼酸C6H8O7中C、H、O三种元素的质量比=(12×6):(1×8)...查看答案和解析>>
科目:初中化学 来源:陕西省西安市2014-2015学年九年级第四次模拟考试化学 题型:科学探究题
碱石灰是CaO和NaOH固体的混合物,常用作干燥剂。碱石灰在空气中久置会吸收空气中的水和二氧化碳而变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。请你参与探究过程:

【查阅资料】①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性。
(1)在操作一实验过程中,同学们发现向样品中加水时放出大量的热。据此实验,下列对样品成分分析正确的是________(填序号)。
A. 一定有NaOH B. 一定有Na2CO3 C. 一定有CaO D. 至少有NaOH、CaO中的一种
(2)在操作二之后所得的固体A中一定含有________。
(3)实验小组的同学继续对溶液B中的溶质进行了探究。
【猜想假设】猜想一:NaOH 猜想二:Na2CO3
猜想三:NaOH和Na2CO3 猜想四:Ca(OH)2和________
【实验验证】为进一步确认溶液B中溶质的成分,做了如下实验。
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,用pH试纸检测滤液的pH | ①__________________; ②pH>7 | 猜想三正确 |
实验步骤①中发生的化学反应方程式是________________________________,其实验目的是________________________________。
【反思评价】对于像碱石灰这样容易变质的物质,保存时需要注意密封保存。
D 碳酸钙 NaOH 产生白色沉淀 CaCl2+Na2CO3=== CaCO3↓+2NaCl 验证并除尽碳酸钠 【解析】(1)由于氧化钙能与水化合生成氢氧化钙放出了大量的热、氢氧化钠溶于水时能够放出大量的热,所以样品中至少有氢氧化钠、氧化钙中的一种.分析选择项,D正确;(2)操作二的名称是过滤,可以把形成的沉淀和溶液分离;氧化钙变质后能够形成的碳酸盐是碳酸钙,氢氧化钠变质后能够形成的碳酸盐是...查看答案和解析>>
科目:初中化学 来源:陕西省西安市2014-2015学年九年级第四次模拟考试化学 题型:单选题
下表是小丽同学根据实验目的所确定的实验方法,其中完全正确的是( )
实验方法 | 实验目的 | 方法1 | 方法2 |
A | 除去铜粉中的铁粉 | 用磁铁吸引 | 加入AgNO3溶液,过滤 |
B | 鉴别硝酸铵和氢氧化钠 | 加入水,观察温度变化 | 加入熟石灰研磨闻气味 |
C | 鉴别二氧化碳和氧气 | 通入CaCl2溶液中,观察现象 | 将燃着的木条放入瓶中,观察现象 |
D | 区分黄铜(铜锌合金)和黄金 | 观察颜色 | 在空气中加热,观察现象 |
A. A B. B C. C D. D
B 【解析】A、用磁铁吸引可以除去铜中的铁,方法1正确,加入AgNO3溶液,过滤,虽然能够除去铁,但是带入新的杂质银,方法2不正确,该选项不完全正确;B、加入水时,溶液温度明显升高的是氢氧化钠,温度明显降低的是硝酸铵,方法1正确,加入熟石灰研磨时,能够产生刺激性气味的是硝酸铵,无明显现象的是氢氧化钠,方法2正确,该选项完全正确;C、通入CaCl2溶液中时,都无明显现象,方法1不正确,用燃着的...查看答案和解析>>
科目:初中化学 来源:江苏省无锡市2018届九年级下学期月考化学试卷 题型:填空题
(1)我们生活在一个丰富多彩的物质世界中,人类的生产、生活和化学密不可分。
(1)用适当的化学符号填空
①能做建筑材料的盐是__________ ②相对分子质量最小的氧化物_______
③光合作用产生的气体是_______ ④最简单的有机物_________
(2)铅蓄电池在生产、生活中使用广泛.其构造示意图如图,回答下列问题:
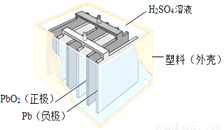
①铅蓄电池充电时是将电能转化为_____能
②铅蓄电池放电过程中,反应的化学方程式为 Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断__(填“增大”、“减小”或“不变”)
③从材料分类角度看,塑料是一类__________材料。 (填“合成”或“复合”)
④废硫酸直接排放会污染环境,可以用熟石灰中和硫酸,写出该反应的化学方程式________。
CaCO3、 H2O、 O2、 CH4 化学能、 增大、 合成 Ca(OH)2+H2SO4=CaSO4+2H2O 【解析】(1)①石灰石的主要成分是碳酸钙,属于盐,能做建筑材料,化学式是CaCO3; ②由两种元素组成,且其中一种是氧的化合物叫氧化物;相对分子质量最小的氧化物是水,化学式是H2O;③光合作用产生的气体是氧气:O2; ④最简单的有机物是甲烷:CH4;(2) ①铅蓄电池充电时是将电...查看答案和解析>>
科目:初中化学 来源:江苏省无锡市2018届九年级下学期月考化学试卷 题型:单选题
在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,没有气泡产生。下列判断正确的是
A. 滤出的固体中一定含铜,可能含铁和镁
B. 滤液中加硝酸银溶液一定有白色沉淀生成
C. 滤液的质量一定增加
D. 滤液中一定含氯化镁、氯化亚铁和氯化铜
B 【解析】金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强。位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。在氯化铜和氯化亚铁的混合溶液中加入一定量的镁粉,镁先与氯化铜反应生成氯化镁和铜,氯化铜完全反应后,镁和氯化亚铁反应生成氯...查看答案和解析>>
科目:初中化学 来源:广东省2018届初三5月月考化学试卷 题型:单选题
从下列对比试验不能得出相应结论的是( )
A. A B. B C. C D. D
C 【解析】A、图中第一个实验是探究铁能生锈是否与氧气有关,第二支试管的铁能与空气据此,第二个实验是探究铁能生锈是否与水有关,故选项实验操作能得出相应结论;B、图示实验,过氧化氢溶液的浓度相同,能说明二氧化锰能加快过氧化氢溶液分解的速率,故选项实验操作能得出相应结论。C、第一个实验二氧化碳不能使石蕊变色,说明二氧化碳不显酸性,第二个实验中二氧化碳和水生成碳酸,碳酸使石蕊变红,不能说明二氧化碳...查看答案和解析>>
科目:初中化学 来源:湖南省2018届九年级第一次模拟考试理综化学试卷 题型:单选题
甲、乙两种物质的溶解度曲线如图所示。下列叙述正确的是( )

A. 当甲中含有少量乙杂质时,可以用将混合物在较高温度配制饱和溶液,冷却后析出甲晶体的办法得到纯甲晶体
B. 将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
C. 将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法
D. t1℃时,甲和乙的饱和溶液各100g,其溶质的质量不相等
A 【解析】A、甲的溶解度受温度影响变化明显,故当甲中含有少量乙杂质时,可以用将混合物在较高温度配制饱和溶液,冷却后析出甲晶体的办法得到纯甲晶体,正确;B、将甲、乙的饱和溶液从t2℃降到t1℃,由于不知道溶液质量的大小,故无法比较析出晶体质量的大小,错误;C、甲的溶解度随温度的升高而增大,将t2℃时甲的饱和溶液变为不饱和溶液,可采取升温的方法,错误;D、t1℃时,甲和乙的溶解度相等,故甲和乙...查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com