
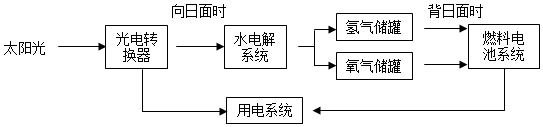
| A. | 该过程中,没有发生化学反应 | |
| B. | 燃料电池系统将化学能转化为电能 | |
| C. | 水的分解反应需要吸收能量 | |
| D. | 该能量转化系统中的水可以回收使用 |
 口算题天天练系列答案
口算题天天练系列答案科目:初中化学 来源: 题型:填空题
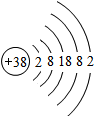 据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:
据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 爱护水资源主要从节约用水和防治水体污染两方面采取相应措施 | |
| B. | 生活中通过煮沸的方法可以降低水的硬度 | |
| C. | 用蒸馏的方法可以将海水淡化 | |
| D. | 水的电解实验说明水是由氢气和氧气组成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将带火星的木条伸入集气瓶中,木条不复燃,则集气瓶中一定不含有O2 | |
| B. | 氦原子和镁原子的最外层电子数相同,则氦原子和镁原子的化学性质相似 | |
| C. | 水电解产生H2和O2,所以水是由氢元素和氧元素组成的 | |
| D. | 二氧化碳通入紫色石蕊溶液后溶液变红,说明二氧化碳具有酸性 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
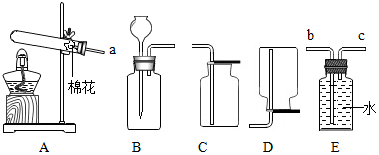 实验操作考试中为了制取氧气和二氧化碳,实验室提供了以下药品和仪器装置,请回答下列问题:
实验操作考试中为了制取氧气和二氧化碳,实验室提供了以下药品和仪器装置,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com