
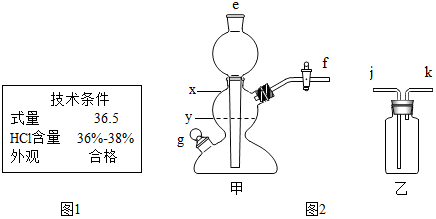
| 溶剂 | 1.0L水 | 1.0L酒精 |
| 溶解度 | 1.0L | 0.5L |
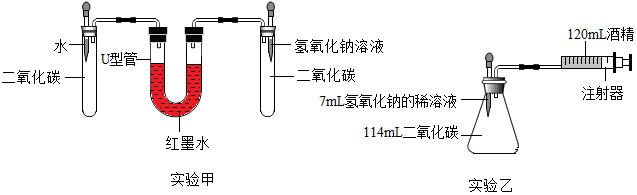
分析 实验一:(1)根据控制反应速率的方法来分析;
(2)根据实验室制取二氧化碳的药品来分析;
(3)根据药品的量的选择来分析;
(4)根据二氧化碳的密度来分析;
(5)根据实验室中制取氢气的原理来分析;
实验二:(1)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(2)根据检验装置气密性可以利用装置内外产生的压强差来验证;
(3)根据氢氧化钠会与二氧化碳反应,二氧化碳会与水反应,但是二氧化碳与氢氧化钠溶液反应后,压强的变化幅度大进行分析;
(4)根据氢氧化钠与二氧化碳反应后装置内的压强减少速度快,但是碳酸钠在酒精中是微溶的进行分析;
(5)根据二氧化碳在水中的溶解度大于酒精中的溶解度进行分析.
解答 解:实验一:(1)为使制备过程中二氧化碳平稳地产生且较纯净,应将该浓盐酸进行稀释,反应物的浓度变小,反应速率减慢;故填:稀释;
(2)在实验室中,通常用大理石或石灰石与稀盐酸反应来制取二氧化碳,粉末状的石灰石与盐酸接触面积过大,反应速率过快;而熟石灰和生石灰与盐酸反应不会生成二氧化碳;故填:b;
(3)选择的液体药品只要是能将固体药品浸没起来即可;故填:y;
(4)二氧化碳的密度比空气大,所以收集二氧化碳时,应该从长管进入;故填:f;j;
(5)在实验室中,用锌粒与稀硫酸反应来制取氢气,同时生成硫酸锌;故填:Zn+H2SO4=ZnSO4+H2↑;
实验二:(1)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;故填:2NaOH+CO2=Na2CO3+H2O;
(2)检验装置气密性可以利用装置内外产生的压强差来验证,所以实验甲装置气密性检查的方法是:往U形管内加入适量的水,连接装置,用手捂住一支试管,观察U形管内液面变化,然后用手捂住另一只试管,再次观察U形管内液面变化;故填:用手紧握左边的试管,U型管内液面会出现右高左低的现象,放开手后,一段时间后回落到原位置,同理检验右侧试管;
(3)氢氧化钠会与二氧化碳反应,二氧化碳会与水反应,但是二氧化碳与氢氧化钠溶液反应后,压强的变化幅度大,所以实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是:右侧液面升高,左侧液面下降,一段时间后,右侧液面缓慢下降,左侧上升,右侧液面仍高于左侧;故填:高于;
(4)氢氧化钠与二氧化碳反应后装置内的压强减少速度快,但是碳酸钠在酒精中是微溶的,出现了白色浑浊的现象,所以将氢氧化钠完全滴入锥形瓶中,注射器会自动向内移动并将酒精推入锥形瓶,活塞的移动速度是先快后慢,故填:B;锥形瓶中出现白色浑浊;
(5)二氧化碳在水中的溶解度大于酒精中的溶解度,碳酸钠在酒精中微溶,现象明显,所以实验乙中,120mL酒精不能换成水;故填:二氧化碳在水中的溶解度大于在酒精中.
点评 本题难度不大,掌握气体的制取与收集方法,在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图是空气中氧气含量的测定装置.试回答:
如图是空气中氧气含量的测定装置.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 的微粒符号O2-;②标出过氧化氢中氧元素的化合价${H}_{2}\stackrel{-1}{{O}_{2}}$,.
的微粒符号O2-;②标出过氧化氢中氧元素的化合价${H}_{2}\stackrel{-1}{{O}_{2}}$,.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com