
分析 (1)根据二氧化碳的质量算出碳酸钠的质量,再用碳酸钠的质量除以样品的质量解答即可;
(2)根据二氧化碳的质量计算出生成的氯化钠的质量,再加上原来的氯化钠质量,除以反应后总溶液质量即可解答.
解答 解:设生成4.4 g CO2需碳酸钠的质量为x,生成氯化钠的质量为y
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 117 44
x y 4.4g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{4.4g}$
∴x=10.6g y=11.7g
纯碱样品中Na2CO3的质量分数=$\frac{10.6g}{11.2g}$×100%=94.6%
反应后溶液中溶质的质量分数=$\frac{11.7g+11.2g-10.6g}{11.2g+93.2g-4.4g}$×100%=12.3%.
答:(1)纯碱样品中的Na2CO3的质量分数是94.6%;(2)反应后所得溶液中NaCl的质量分数是12.3%.
点评 解答本题容易出错的地方是计算反应后所得溶液中NaCl 的质量分数时,容易忽略原来的氯化钠质量.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题

| A. | 10℃时,将30 g A物质放入50 g水中充分搅拌后所得溶液的质量为80 g | |
| B. | 将30℃时,A、B、C三种物质的饱和溶液降温到10℃,C的溶质质量分数保持不变 | |
| C. | 升高温度可以使C的不饱和溶液转变成饱和溶液 | |
| D. | 采用冷却热饱和溶液的方法可以从A、B的混合物中分离A物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
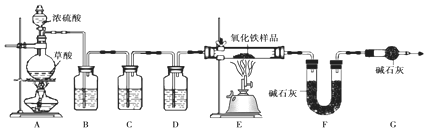
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 稀盐酸的质量/g | 20g | 40g | 60g |
| 生成气体的质量/g | 2.2 | m | 5.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
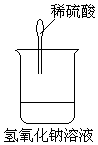 小华同学用如图所示装置进行中和反应实验,反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
小华同学用如图所示装置进行中和反应实验,反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原混合气体中一定含有H2、CO、CO2 | |
| B. | 原混合气体中一定没有CO2,一定含有H2、CO | |
| C. | 原混合气体中一定含有H2、CO2,可能含有CO | |
| D. | 原混合气体中一定含有CO、CO2,可能含有H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com