
分析 (1)根据二氧化碳与氢氧化钠反应生成了碳酸钠和水,反应没有现象,无法判断反应的进行.二氧化碳是气体,生成物中没有气体,可以借助压强的变化来判断.解答本题时,认真观察图示,分析实验装置设计的原理及依据、设计思路等,能否以此判定二氧化碳与氢氧化钠是否发生反应;
(2)①根据氢氧化钠能够和硫酸反应,再滴加硫酸铜溶液不会产生沉淀说明氢氧化钠反应了分析;
③根据氢氧化钠溶液加水会使溶液的pH变小,但不会等于或小于7进行分析.
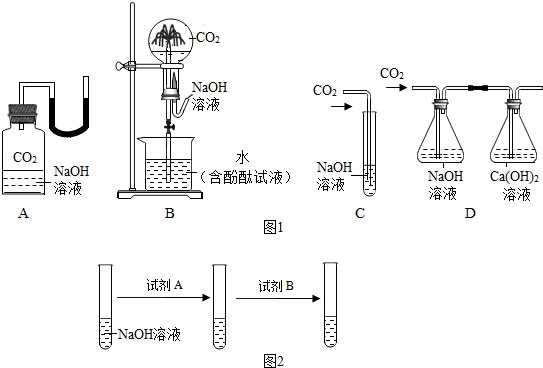
解答 解:(1)B、装置中的烧瓶充满了二氧化碳气体,通过胶头滴管加入少量的氢氧化钠,二氧化碳与氢氧化钠反应生成了碳酸钠和水,瓶内压强减小,形成喷泉,现象明显,故方案可行;
A、瓶内的二氧化碳与氢氧化钠反应生成了碳酸钠和水,压强减小,在大气压的作用下,U形管内水柱左侧升高甚至进入瓶中,现象明显,故方案可行;
C、二氧化碳与氢氧化钠反应生成了碳酸钠和水,反应没有现象,无法判断反应的进行,故方案不可行;
D、通入二氧化碳时,二氧化碳被左侧的锥形瓶中石灰水吸收了,右锥形瓶内没有现象,因此不能判断二氧化碳与氢氧化钠发生了反应,故方案不可行;
故选:CD;
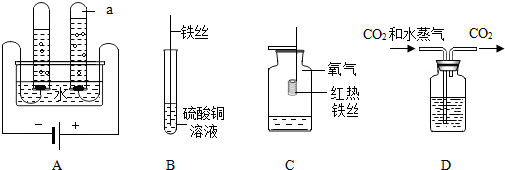
(2)①氢氧化钠和足量的稀硫酸反应后会消失,因此滴加硫酸铜溶液不会产生蓝色沉淀,因为氢氧化钠和硫酸铜反应会产生氢氧化铜沉淀和硫酸钠,反应的方程式为:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;
②因为稀释氢氧化钠溶液时,碱性减弱,溶液的pH变小,但是不能等于或小于7,如果pH小于7,说明氢氧化钠和硫酸发生了化学反应,氢氧化钠消失,最后的溶液显酸性,可以证明氢氧化钠发生了化学反应.
故答案为:(1)CD;
(2)①足量的硫酸溶液或足量的稀硫酸,2NaOH+Cu SO4=Na2SO4+Cu(OH)2↓;
②因为稀释氢氧化钠溶液时,碱性减弱,溶液的pH变小,但是不能等于或小于7,如果pH小于7,说明氢氧化钠和盐酸发生了化学反应.
点评 本题属于实验方案评价题,主要考查了二氧化碳与氢氧化钠的反应及氢氧化钠和硫酸反应的知识,解题的关键是:认真观察图示,获取相关信息,结合二氧化碳与氢氧化钠的反应的知识,分析实验的目的、原理,设计思路,现象是否明显等,从而对方案进行评价.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 使用弹簧测力计时,应先调零,后进行测量 | |
| B. | 稀释浓硫酸时先将浓硫酸倒入烧杯中,后将水沿着烧杯壁慢慢倒入浓硫酸中 | |
| C. | 使用显微镜观察细胞时,先调节细准焦螺旋,后调节粗准焦螺旋 | |
| D. | 实验室制取氧气,停止加热时,应先熄灭酒精灯,再把导管移出水面 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
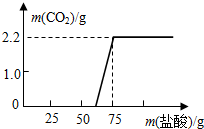 实验室中久置的NaOH会因为吸收空气中的CO2而变质.为了测定实验室中久置的NaOH的变质程度,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,确定样品中NaOH的变质程度.若实验测得加入稀盐酸的质量与产生的CO2气体的质量关系如图所示.请根据图象分析计算:
实验室中久置的NaOH会因为吸收空气中的CO2而变质.为了测定实验室中久置的NaOH的变质程度,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,确定样品中NaOH的变质程度.若实验测得加入稀盐酸的质量与产生的CO2气体的质量关系如图所示.请根据图象分析计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
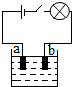 小李同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按下图所示的装置进行实验,实验结果记录如下表:
小李同学查阅资料了解到化合物根据导电性的不同,可分为电解质和非电解质两大类.其中在水溶液里或熔化状态下能够导电的化合物叫做电解质,在水溶液里或熔化状态下都不能导电的化合物叫做非电解质.于是他以食盐、硝酸钾、蔗糖、氢氧化钠和硫酸铜为材料,按下图所示的装置进行实验,实验结果记录如下表:| 物质 导电性 状态 | 食盐NaCl | 硝酸钾KNO3 | 蔗糖C12H22O18 | 氢氧化钠NaOH | 硫酸铜CuSO4 |
| 固态 | × | × | × | × | × |
| 熔化状态 | √ | √ | × | √ | √ |
| 水溶液 | √ | √ | × | √ | √ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用活性炭将硬水软化 | |
| B. | 用水除去生石灰中混有的碳酸钙 | |
| C. | 用点燃的方法除去CO2中少量的CO | |
| D. | 加入氧化镁除去硫酸镁溶液中含有的少量硫酸(氧化镁难溶于水) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
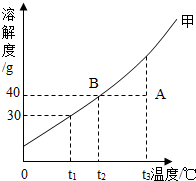 如图是固体物质甲的溶解度曲线,请据图回答下列问题.
如图是固体物质甲的溶解度曲线,请据图回答下列问题. 查看答案和解析>>
科目:初中化学 来源:2017届山东省菏泽市九年级中考预测题(一)化学试卷(解析版) 题型:选择题
下列各组离子能在指定溶液中大量共存的一组是
A.在稀盐酸中:Ba2+、CO3 2- 、Zn2+ B.在氢氧化钠溶液中:H+ 、Mg2+ 、 Cl-
C.在氯化钠溶液中:K+ 、Ca2+ 、NO3 - D.在硝酸铵溶液中:Na+ 、Cu2+ 、OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com