
| ����ϡ��������/mL | 40 | 80 | 120 | 160 | 200 |
| �ձ���ʣ����������/g | 12 | m | 5.6 | 4 | 4 |

���� ��1����������ϡ���ᷴӦ�������������������������μ���ϡ���������Ȼ���٣�����ǰ���μ��������ϡ����ʱ��������������Ӧ����ȣ������m��������
��2�������������������ݻ�ѧ����ʽ������������������Ȼ���������������
��� �⣺��1������ϡ���ᷴӦ�������������������������μ���ϡ���������Ȼ���٣�����ǰ���μ��������ϡ����ʱ��������������Ӧ����ȣ�����m=12g-$\frac{12g-5.6g}{2}$=8.8g��
��2�����Կ�ʼ�ձ��й������ʵ�����Ϊ��12g+3.2g=15.2g��������4g��������������Ϊ��15.2g-4g=11.2g��
��μӷ�Ӧ������������Ϊx
Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2
160 112
x 11.2g
$\frac{160}{x}$=$\frac{112}{11.2g}$
x=16g
����������������������$\frac{16g}{16g+4g}$��100%=80%��
�ʴ�Ϊ����1��8.8��
��2��80%��
���� ������Ҫ�����˻�ѧ����ʽ�ļ��㣬�ѶȲ���ע�����Ĺ淶�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 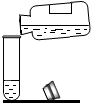 | B�� |  | C�� | 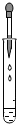 | D�� | 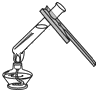 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
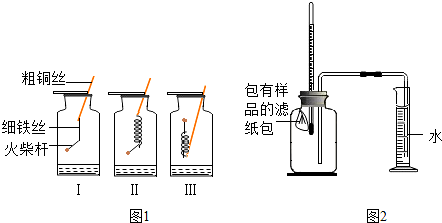
| ��� | ��Ʒ | ��Ͳ��ʼ����/mL | ��Ͳ���ն���/mL | ����ʱ��/min |
| 1 | 1g���ۡ�0.2g̼��10��ˮ | 100 | 72 | Լ120 |
| 2 | lg���ۡ�0.2g̼��10��ˮ������NaCl | 100 | 72 | Լ70 |
| 3 | / | / | / |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��һ�� | �ڶ��� | ������ | |
| ��ȡ�Ͻ������/g | 10 | 10 | 20 |
| ����ϡ���������/g | 100 | 120 | 80 |
| ��������������/g | 0.2 | 0.2 | 0.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2Fe+6HCl�T2FeCl3+3H2�� | B�� | Fe2O3+3H2SO4�TFe2��SO4��3+3H2O | ||
| C�� | Mg+2NaOH�TMg��OH��2��+2Na | D�� | Na2CO3+2HNO3�T2NaNO3+H2CO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
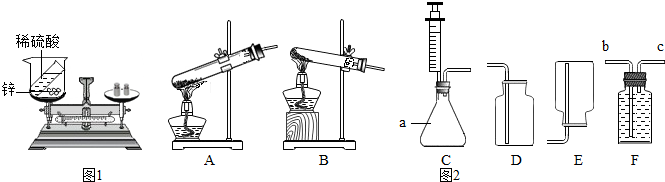
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
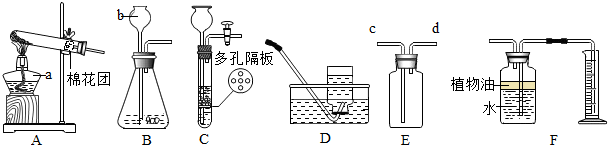
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com