
【题目】(1)向含有 NaOH 和 Ca(OH)2 的混合溶液中缓缓通入 CO2直到过量。其现象为:开始出现沉淀,后来沉淀逐渐溶解。请按照先后顺序写出相应反应的化学方程式:
①_____________ ②_________
③![]() ④_________
④_________
(2)高氯酸(HClO4)是最强酸。现有一种不常见的氯的化合物叫做高氯酸氯,其分子中氯的质量分数为 0.526,且每个分子中含有 4 个氧原子。
①高氯酸氯的化学式为___________,物质类别可归为 __________。
②高氯酸氯在室温下即发生分解,形成 Cl2、O2和另一种氯的氧化物。已知该反应的化学方程式中3种产物的化学计量数相同。请写出该分解反应的化学方程式:___________。
(3)医药上可用石膏来固定骨折部位。石膏有熟石膏(CaSO4·![]() H2O,一种白色粉末)和生石膏(CaSO4·2H2O,一种坚硬的固体)两种,固定骨折的石膏是__________________。(填化学式)。固定时发生反应的化学方程式__________________。
H2O,一种白色粉末)和生石膏(CaSO4·2H2O,一种坚硬的固体)两种,固定骨折的石膏是__________________。(填化学式)。固定时发生反应的化学方程式__________________。
(4))CO与PdCl2溶液反应产生黑色金属钯粉末(反应中有水参加),用此来检测 CO 对环境的污染情况,此反应的化学方程式为:________,反应中中可能看到的现象是________。
【答案】![]()
![]()
![]() Cl2O4 氧化物
Cl2O4 氧化物 ![]() CaSO4·
CaSO4·![]() H2O
H2O ![]()
![]() 溶液中生成黑色沉淀
溶液中生成黑色沉淀
【解析】
(1)通入二氧化碳后,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,二氧化碳与氢氧化钠反应生成碳酸钠和水,继续通入二氧化碳,二氧化碳与碳酸钠、水反应生成碳酸氢钠,二氧化碳与碳酸钙、水反应生成碳酸氢钙,碳酸氢钙溶于水,因此看到沉淀溶解,据此书写化学方程式;
故答案为:![]() ;
;![]() ;
;![]() 。
。
(2)①、设氯原子个数为n,则氯元素质量分数=![]() ,n=2,所以化学式为Cl2O4,由两种元素组成,且一种元素为氧元素,所以属于氧化物;
,n=2,所以化学式为Cl2O4,由两种元素组成,且一种元素为氧元素,所以属于氧化物;
故答案为:Cl2O4;氧化物。
②、反应为分解反应,所以反应物只有高氯酸氯,若只有1分子高氯酸氯参与反应,生成1分子氯气和1分子氧气,还剩余2个氧原子,无法形成含氯元素的氧化物,因此高氯酸氯最少有2分子参与反应,此时反应物有4个氯原子和8个氧原子,生成物为1分子氯气和1分子氧气,含有了2个氯原子和2个氧原子,还应有2个氯原子和6个氧原子,因此剩余氧化物化学式为Cl2O6,所以化学方程为高氯酸氯分解生成氯气、氧气和六氧二氯,书写化学方程式注意配平;
故答案为:![]() 。
。
(3)骨折时骨折部位需要固定,此时石膏应为粉末状,便于制成膏状物涂覆到受伤部位,然后再进行包扎固定,因此选用熟石膏,化学式为![]() ;熟石膏可以吸收水分变为生石膏,变为固体,达到固定受伤部位的目的,因此是熟石膏与水反应生成生石膏,书写化学方程式注意配平;
;熟石膏可以吸收水分变为生石膏,变为固体,达到固定受伤部位的目的,因此是熟石膏与水反应生成生石膏,书写化学方程式注意配平;
故答案为:![]() ;
;![]() 。
。
(4)反应物有一氧化碳、氯化钯和水,产物目前有钯,产物还应有氢元素、氯元素、碳元素和氧元素,氯化钯中钯元素显+2价,钯单质中钯元素为0价,化合价降低,所以还应出现一种元素化合价升高,在反应物中只有碳元素符合此条件,与氧元素结合生成二氧化碳,剩余氢元素与氯元素可以结合生成氯化氢,因此反应为一氧化碳、氯化钯和水反应生成钯、二氧化碳和氯化氢,据此书写化学方程式,注意配平;反应前为溶液,生成钯单质为黑色固体,因此可以看到溶液中有黑色沉淀生成;
故答案为:![]() ;溶液中生成黑色沉淀。
;溶液中生成黑色沉淀。


科目:初中化学 来源: 题型:
【题目】如图是a、 b两种固体物质(不含结晶水)的溶解度曲线。t1°C时,分别向盛有10g水的两支试管中,加入等质量的a、b两种固体物质,使其充分溶解。可观察到如图所示的现象。
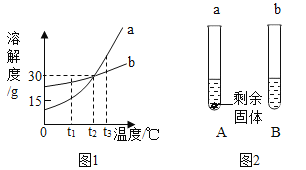
(1)t1°C时,_____________(填“A”或“B”)试管中的溶液一定是饱和溶液。
(2)当温度为___________时,a、b两物质 的溶解度相等。
(3)将t3°C时a、 b两种物质的饱和溶液降温到t1°C,则所得溶液中溶质的质量分数大小关系是: a________b(填“>”、 “<”或“=”)。
(4)向100g t2°C的水中加入35g a固体,发现全部溶解,一段时间后又有部分a的晶体析出,则析出晶体的质量是____________g。
(5)按图所示装置,将液体x注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是_______________。
选项 | X | Y |
|
A | 水 | 氧化钙 | |
B | 水 | 硝酸铵 | |
C | 浓硫酸 | 水 | |
D | 稀硫酸 | 镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学利用锌、氧化铜和稀硫酸制取铜,他设计了两套方案,方案Ⅰ:利用锌与足量稀硫酸反应制氢气,氢气还原氧化铜;方案Ⅱ:氧化铜溶于稀硫酸生成硫酸铜,然后用锌与硫酸铜反应制备铜。下列关于方案Ⅰ和Ⅱ的评价不正确的是( )
A.方案Ⅱ比方案Ⅰ操作简便
B.等质量的锌,相同条件下在方案Ⅰ和方案Ⅱ中制得的铜的质量相同
C.等质量的H2SO4参加反应,方案Ⅰ制取铜的质量比方案Ⅱ的少
D.为了加快锌与稀硫酸反应,可以在溶液中加入少量氧化铜
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向20g某赤铁矿石(主要成分是Fe2O3,假设杂质不溶于水,也不与酸反应)样品中,逐渐加入稀硫酸,充分反应。实验相关数据如图所示。
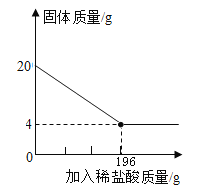
(1)20g赤铁矿石样品中氧化铁的质量为______g
(2)计算试验中所用稀硫酸溶质的质量分数(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌可乐由水、白砂糖、焦糖色素(使可乐显黑褐色)、磷酸(H3PO4)等,按一定比例混合并压入二氧化碳配制而成。某同学为了探究可乐的成分及其含量,进行如下实验。
实验一 可乐中二氧化碳的定性检验
(1)请完成下表:
实验步骤 | 实验现象 | 结论 |
打开一塑料瓶装可乐,塞上带导管的橡胶塞,把导管插入 (填化学式)溶液中 | 观察到 | 可乐中含有二氧化碳 |
实验二 可乐中磷酸的定量测定
测定过程如下:
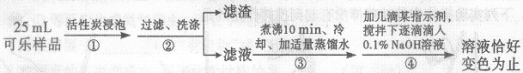
(2)步骤①用活性炭浸泡的目的是 。
(3)步骤③煮沸10分钟的目的是除尽滤液中的 。
(4)已知步骤④反应的化学方程式为H3PO4+NaOH=NaH2PO4+H2O,测得共消耗0.1%的NaOH溶液20g,忽略可乐中其它成分对测定结果的影响,计算可乐中磷酸的含量(以g/L为单位。相对分子质量:H3PO4—98;NaOH—40),写出计算过程。
(5)如果步骤②缺少洗涤,则测定结果 (填“偏高”“不变”或“偏低”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中甲、乙分别表示两种固体物质(不含结晶水)的溶解度曲线,试根据图中曲线判断下列说法正确的是( )
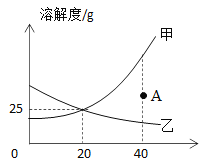
A.图中A点表示甲、乙两种物质在40℃时均达到饱和
B.甲、乙两种饱和溶液,当温度从40℃降至20℃时,一定析出相同质量的晶体
C.将40℃等质量的甲、乙两种饱和溶液降温至20℃后,剩余溶液中的溶剂的质量关系为甲小于乙
D.0℃时,甲、乙具有相同的溶解度
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D、E、F均为初中化学常见的物质,且均含同一种元素。B、C组成元素相同,D、E、F的水溶液均呈碱性,A为单质,F常用作改良酸性土壤。它们之间存在如图所示的转化关系,“一”表示两种物质之间可以相互反应,“→”表示一种物质可生成另一种物质。请回答下列问题:
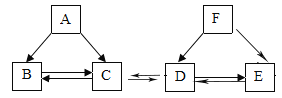
(1)A物质的名称是_____。
(2)F转化为E的化学方程式为_____。
(3)除去E中混有的少量D的方法是_____。
(4)C转化为B的基本反应类型为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一种不纯的二氧化碳气体,其中可能混有O2、CO中的一种。现取这种气体4.4克,与炽热的焦炭充分反应后,气体质量增加到5.8克。则混入的气体是( )
A.O2
B.CO
C.二者皆无
D.无法判断
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列叙述中正确的是( )
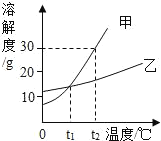
A. 甲物质的溶解度大于乙物质的溶解度
B. t1℃时,甲、乙两物质饱和溶液的溶质质量一定相等
C. t2℃时,将20g乙物质放入100g水中,所得溶液的质量为120g
D. t2℃时,等质量甲、乙两物质的饱和溶液降温到t1℃,析出晶体质量甲>乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com