
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)盐酸和锌反应生成氯化锌和氢气,反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
(2)盐酸和氧化锌反应生成氯化锌和水,反应的化学方程式为:ZnO+2HCl═ZnCl2+H2O.
(3)盐酸和氢氧化锌反应生成氯化锌和水,反应的化学方程式为:Zn(OH)2+2HCl═ZnCl2+2H2O.
(4)盐酸和碳酸锌反应生成氯化锌、水和二氧化碳,反应的化学方程式为:ZnCO3+2HCl=ZnCl2+H2O+CO2↑.
从上述反应方程式可知制取氯化锌的方法有多种.
故答案为:(1)Zn+2HCl═ZnCl2+H2↑;(2)ZnO+2HCl═ZnCl2+H2O;(3)Zn(OH)2+2HCl═ZnCl2+2H2O;(4)ZnCO3+2HCl=ZnCl2+H2O+CO2↑.氯化锌.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 滤渣中一定没有Fe | |
| B. | 滤渣中一定有Ag,可能有Cu | |
| C. | 滤液中一定含有Fe(NO3)2,一定没有有AgNO3 | |
| D. | 滤液一定有Fe(NO3)2和Cu(NO3)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 一定有K2SO4 | B. | 一定有NaCl | C. | 一定有Na2CO3 | D. | 可能有NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 浓盐酸和食盐水 | B. | 浓硫酸和石灰水 | ||
| C. | 液氧和浓盐酸 | D. | 液氧和氢氧化钠的浓溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
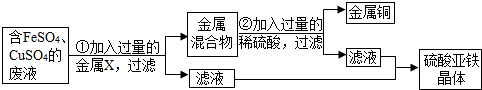
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 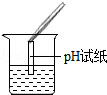 | 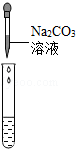 | 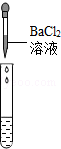 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com