
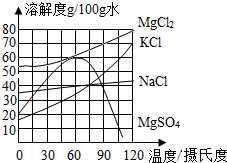
 食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富,通过晾晒海水可以得到粗盐和卤水.如图所示为NaCl及卤水主要成分的溶解度曲线图.
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富,通过晾晒海水可以得到粗盐和卤水.如图所示为NaCl及卤水主要成分的溶解度曲线图.分析 (1)食盐的溶解度受温度影响变化不大,利用海水晒盐,是利用了蒸发结晶的原理,据此进行分析解答.
(2)根据在60℃时KCl的溶解度分析判断回答;
(3)根据在90℃时,MgCl2溶液溶解度计算;
(4)根据MgCl2、KCl和MgSO4三种物质的溶解度随温度变化的情况分析回答.
解答 解:(1)食盐的溶解度受温度的影响小,从食盐溶液中获得食盐主要利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来.
(2)由KCl的溶解度曲线可知,在60℃时,KCl的溶解度是35.5g,100g水中加入80gKCl,充分搅拌后观察到的现象是有部分KCl未溶解,所形成的溶液是饱和溶液.
(3)由MgCl2的溶解度曲线可知,在90℃时,MgCl2溶液的溶解度是70g,在90℃时,MgCl2饱和溶液的浓度最大,为:$\frac{70g}{100g+70g}×100%$;
(4)将90℃时,MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至30℃时,由于MgSO430℃时溶解度大于90℃时的溶解度,没有晶体析出.
故答案为:(1)利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来.(2)有部分KCl未溶解,饱和溶液;(3)$\frac{70g}{100g+70g}×100%$;(4)MgSO4.
点评 解答本题关键是要知道海水晒盐的原理,溶解度曲线的意义以及饱和溶液与不饱和溶液的判断及转化等知识.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:选择题
| A. | 该反应是置换反应 | B. | X可能是铁 | ||
| C. | 金属活动性X>Ag | D. | X表面有固体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化铝属于碱 | |
| B. | NaAlO2中铝元素的化合价为+3价 | |
| C. | 向氯化铝溶液中逐滴加入过量的氢氧化钠溶液,先产生白色沉淀,后沉淀不消失 | |
| D. | 向稀盐酸中加入氢氧化铝,发生中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若样品不含任何杂质,则m<1.8 | |
| B. | 若m=1.8,则样品中一定含有杂质A,可能含有固体KOH | |
| C. | 若m>1.8,则样品中一定含有固体KOH,可能含有杂质A | |
| D. | 若样品中不含A,则盐酸的溶质质量分数可能为4% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com