
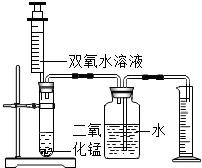
 某化学兴趣小组的同学设计了如图所示的装置,探究影响化学反应速率的因素.
某化学兴趣小组的同学设计了如图所示的装置,探究影响化学反应速率的因素.| 实验 序号 | H2O2溶液 的浓度/% | H2O2溶液 的体积/mL | MnO2的 用量/g | 温度/℃ | 收集O2的体积/mL | 反应所需 的时间/s |
| ① | 5 | 2 | 0.1 | 20 | 4 | 18 |
| ② | 10 | 2 | 0.1 | 20 | 4 | 6 |
| ③ | 30 | 8 | / | 40 | 2 | 64 |
| ④ | 30 | 8 | / | 60 | 2 | 25 |
分析 (1)注射器能够控制过氧化氢的使用量;读数时,视线要与凹液面的最低处保持水平;
(2)①②是过氧化氢浓度不同而其他条件相同,这种设计是验证反应物浓度对反应速度的影响;③④则是温度不同其他条件相同,是对温度影响化学反应速度的探究.
(3)反应物越浓在溶液中离子的密度会更大,离子间结合的机会更多,分析时应从微观离子着手.
解答 解:(1)如图装置中使用注射器的可以随时控制过氧化氢的使用量.给量筒中的液体读数时,视线要与凹液面的最低处保持水平;
(2)从表中分析可知:①②是过氧化氢浓度不同而其他的反应时各种量均相同,可知这一过程是考查反应物的浓度与反应速度的关系.;③④则是温度不同其他条件相同,明显是对温度影响化学反应速度的探究.
(3)反应物浓度大时溶液中的离子数量较多,反应的接触面较大反应速度自然变快.
故答案是:(1)能控制产生氧气的速率(或能控制过氧化氢溶液的使用量);液体凹液面最低处保持水平.
(2)反应物浓度(或溶质的质量分数);温度越高,反应速率越快.
(3)反应物浓度越大,单位体积内微观粒子数目就越多,相互接触发生反应的几率就越大.
点评 本题通过实验探究的方式探究了影响化学反应速度影响的因素,利用控制变量的方法进行实验探究,培养了学生分析问题解决问题的能力,认识了对化学反应速度影响的因素.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| M的质量/g | S的质量/g | M2S的质量/g | |
| 甲 | 6.0 | 2.5 | 7.5 |
| 乙 | 7.0 | 1.5 | 7.5 |
| A. | 64 | B. | 56 | C. | 32 | D. | 23 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙醇 酒精 CH3OH | B. | 碳酸氢钠 小苏打 NaHCO3 | ||
| C. | 氧化钙 熟石灰 CaO | D. | 氢氧化钠 纯碱 NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com